|
|
| |
ULTRAFILTRAZIONE GLOMERULARE
Come
detto, il processo di ultrafiltrazione del plasma avviene nel glomerulo.
L'ultrafiltrato che si forma (circa
Il processo di ultrafiltrazione glomerulare avviene, come in tutti i distretti capillari, tramite un "gioco di pressioni", cioè dal bilancio tra le forze che la favoriscono e quelle che la ostacolano. Prima di analizzare più da vicino queste forze e la dinamica dell'ultrafiltrazione, dobbiamo considerare alcuni parametri riguardanti la particolare irrorazione renale, le pressioni vigenti nel circolo renale stesso e la permeabilità selettiva del filtro glomerulare.
FLUSSO EMATICO RENALE
Nell'uomo
medio di
La particolarità del flusso sanguigno attraverso il nefrone è legata al fatto che esso possiede un duplice letto capillare: 1) il glomerulo e 2) i capillari peritubulari. Il primo è alimentato dall'arteriola afferente; tra il glomerulo ed i capillari peritubulari è interposta l'arteriola efferente, che oppone una considerevole resistenza al flusso ematico. Ne consegue che quello dei capillari glomerulari è un letto capillare ad alta pressione, mentre quello dei capillari peritubulari è un letto a bassa pressione. A causa dell'elevata pressione vigente nei suoi capillari, il glomerulo funziona in modo assai simile a quello dell'estremo arteriolare dei capillari dei tessuti, determinando una continua filtrazione di liquido dal glomerulo alla capsula del Bowman. D'a 555c24f ltra parte, il sistema dei capillari peritubulari, in virtù della sua bassa pressione, funziona allo stesso modo dell'estremo venulare dei capillari tessutali, richiamando continuamente liquido all'interno dei capillari.
PRESSIONI NEL CIRCOLO RENALE
Nelle varie sezioni della circolazione renale vigono pressioni diverse. Inizialmente, a livello delle grosse arterie arciformi (rami collaterali delle arterie interlobari, a loro volta collaterali dell'arteria renale), la pressione è di circa 100 mmHg, mentre nelle vene, che alla fine convogliano il sangue refluo dai nefroni, è pari a circa 8 mmHg. Le due zone di maggior resistenza al flusso sanguigno sono: 1) le piccole arterie renali e l'arteriola afferente e 2) l'arteriola efferente. Nelle prime la pressione, da 100 mmHg dell'estremo iniziale, scende nel glomerulo a circa 60 mmHg. A livello dei capillari peritubulari la pressione scende ad un valore medio di 13 mmHg. Si può capire, allora, che il glomerulo operando ad una pressione di 60 mmHg, promuove una rapida filtrazione di liquido, mentre i capillari peritubulari lavorando a 13 mmHg, permettono un rapido assorbimento di liquido per effetto dell'elevata pressione osmotica del plasma.
PERMEABILITÀ DEL FILTRO GLOMERULARE
L'ultrafiltrato glomerulare passa, come detto, attraverso tre differenti strati prima di entrare nella capsula del Bowman (endotelio capillare; membrana basale glomerulare e strato dei podociti); ciascuno di questi strati è notevolmente più poroso di una comune membrana capillare, il che rende ragione dell'enorme volume di filtrato glomerulare che si può formare al minuto. Nonostante il suo alto grado di permeabilità, il filtro glomerulare possiede una capacità selettiva estremamente elevata per quanto riguarda le dimensioni delle molecole di cui permette il passaggio.
In generale, la permeabilità del filtro per sostanze di differenti pesi molecolari (espressa dal rapporto tra la concentrazione della sostanza disciolta nel filtrato e la concentrazione plasmatica della medesima) è approssimativamente la seguente:
|
Peso molecolare |
Permeabilità |
Sostanze tipo |
|
|
|
Inulina |
|
|
|
Proteina di dimensioni molto piccole |
|
|
|
Albumina |
Questi valori ci indicano che con un peso molecolare di 5.200 la sostanza disciolta filtra tanto agevolmente quanto l'acqua, ma con un peso molecolare di 69.000 può filtrare solo lo 0,5% della sostanza. Si noti che il peso molecolare della più piccola proteina plasmatica, l'albumina, è di 69.000: ciò vuol dire che il filtro glomerulare è pressoché completamente impermeabile alle proteine plasmatiche, ma è altamente permeabile a tutte le altre sostanze normalmente presenti nel plasma. Esistono due ragioni fondamentali dell'elevato grado di selettività molecolare del filtro glomerulare. In primo luogo, la membrana basale, che funge da vero setto filtrante, si comporta come se avesse dei pori (funzionali) di 5-7,5 nm, i quali sono abbastanza grandi da permettere, quindi, il passaggio di molecole con diametro fino a circa 8 nm. Si tenga presente, tuttavia, che il diametro dell'albumina è di solo 6 nm, cioè inferiore a quello dei pori. C'è, dunque, un altro fattore, oltre alle dimensioni molecolari ed alla forma, che determina la permeabilità del filtro glomerulare alle macromolecole. Questo fattore è dato dalle forti cariche elettriche negative presenti a livello delle lamine rare e dello strato di proteoglicani che riveste i pori nelle loro parti a livello della membrana basale. Anche le proteine plasmatiche hanno forti cariche negative, sicché la repulsione elettrostatica da parte delle pareti dei pori e delle lamine impedisce, in pratica, a tutte le molecole di peso molecolare superiore a 69.000 di passare.
L'ultrafiltrato glomerulare ha, quindi, quasi esattamente la stessa composizione liquido che dall'estremo arteriolare dei capillari filtra negli spazi interstiziali in tutti gli altri tessuti. È privo di globuli rossi e contiene circa lo 0,03 % di proteine, cioè all'incirca 1/240 delle proteine del plasma. Anche per quanto riguarda gli elettroliti e gli altri soluti la composizione dell'ultrafiltrato glomerulare è simile a quella del liquido interstiziale. Però, per il fatto che vi sono pochi ioni proteici a carica negativa, si verifica che nell'ultrafiltrato, per l'effetto Donnan , la concentrazione di altri ioni negativi (tra cui cloro e bicarbonato) risulta più alta del 5% che nel plasma, mentre quella degli ioni positivi più bassa del 5%.
Concludendo, possiamo dire che l'ultrafiltrato glomerulare può essere considerato praticamente uguale al plasma, salvo che non contiene significative quantità di proteine.
EFFETTO DONNAN: effetto di trattenimento di cariche elettriche positive (soprattutto sodio) da parte delle proteine plasmatiche, che sono caricate negativamente.
DINAMICA DELL'ULTRAFILTRAZIONE GLOMERULARE
L'ultrafiltrazione glomerulare avviene, come detto, per effetto delle stesse forze che sono responsabili della filtrazione di liquido attraverso qualsiasi altro capillare ad alta pressione dell'organismo. Quindi, l'ultrafiltrazione dipende dal bilancio tra le forze che la favoriscono da una parte e quelle che la ostacolano dall'altra. Analizziamo, ora, tali forze.
Pressione idrostatica dei capillari glomerulari. È la pressione ematica che mediamente vige all'interno dei capillari glomerulari; questa pressione promuove la filtrazione attraverso la membrana glomerulare. È stata misurata direttamente soltanto nel ratto, in cui il valore medio è di 45 mmHg. Da varie misurazioni indirette, nel cane, è stata calcolata tra i 55 ed i 70 mmHg. Nell'uomo, tenuto conto della mole corporea, si può quindi assumere, come valore medio approssimato, quello di 60 mmHg, tenendo tuttavia presente che questo valore può, come vedremo, aumentare o diminuire considerevolmente in differenti condizioni.
Pressione colloidosmotica nella capsula del Bowman. Anche questa pressione promuove la filtrazione glomerulare; tuttavia, normalmente una quota molto piccola di proteine passa nel filtrato glomerulare e quindi questo fattore non ha alcun effetto significativo e viene di solito considerato pari a zero.
Pressione idrostatica della capsula del Bowman. Questa pressione si oppone alla filtrazione. In animali da esperimento sono state eseguite sue misurazioni mediante micropipette. In base a queste ricerche, si valuta che la pressione capsulare nell'uomo sia di circa 18 mmHg.
Pressione colloidosmotica delle proteine plasmatiche. Anche questa pressione si oppone alla filtrazione. Poiché all'incirca un quinto del plasma dei capillari glomerulari filtra nella capsula del Bowman, nel passaggio del sangue da un'estremità all'altra del glomerulo la concentrazione plasmatica delle proteine aumenta di circa il 20%. Se, quindi, la pressione colloidosmotica del sangue che entra nei capillari è, come di norma, pari a 28 mmHg, quando il sangue raggiunge l'estremo terminale dei capillari essa risulta aumentata a circa 36 mmHg; perciò la pressione colloidosmotica media nei capillari glomerulari può essere valutata intorno a 32 mmHg.
La pressione di filtrazione (Pf) è, quindi, il valore netto della pressione che spinge il liquido attraverso la membrana glomerulare ed è pari alla pressione glomerulare (Pg) meno la somma della pressione colloidosmotica glomerulare (p g) e della pressione capsulare (Pc):
Pf = Pg - (p g+ Pc) Pf = 60 - (32 + 18) = 10 mmHg
La normale pressione di filtrazione è, quindi, di circa 10 mmHg (Fig.13).
VELOCITÀ DI FILTRAZIONE GLOMERULARE
Per velocità di filtrazione glomerulare si intende la quantità di filtrato che si forma in un minuto in tutti i nefroni di entrambi i reni. Questo valore dipende non solo dalla pressione di filtrazione, ma anche dalla superficie glomerulare filtrante (numero di glomeruli funzionanti) e dalla permeabilità della membrana filtrante (membrana basale). In condizioni fisiologiche l'una e l'altra sono costanti e possono, quindi, essere rappresentate da una costante (Kf) detta coefficiente di ultrafiltrazione. Perciò la velocità di filtrazione glomerulare (VFG) risulta uguale al prodotto della pressione di filtrazione glomerulare per il coefficiente di ultrafiltrazione:
VFG = Kf X Pf = 125 ml/min
quindi
In
linea teorica
CALCOLO DELLA VELOCITÀ DI FILTRAZIONE GLOMERULARE
La misura della VFG permette di valutare la funzionalità glomerulare: ha pertanto una importanza pratica notevole. Per la sua determinazione si usano metodi indiretti, basati sulle seguenti considerazioni.
Se nel
plasma arterioso è presente una qualunque sostanza alla concentrazione P
(mg/ml), la velocità Vf (mg/min) con cui questa sostanza viene
filtrata dal glomerulo in un minuto (carico filtrato), è data ovviamente
dal prodotto della sua concentrazione plasmatica arteriosa per il volume di
plasma filtrato in un minuto, cioè per
Vf = P X VFG
Analogamente la velocità di escrezione (Ve) della stessa sostanza con le urine (carico escreto) è data dal prodotto della sua concentrazione urinaria U (mg/min) per il flusso urinario F (ml/min). Perciò:
Ve = U X F
Se la sostanza in questione ha la proprietà di venir filtrata completamente, ma di non venir né riassorbita né secreta dal tubulo, allora tutta quella filtrata in un minuto viene, in pari tempo, escreta con le urine: cioè, la velocità della sua filtrazione è uguale a quella della sua escrezione:
Vf = Ve P X VFG = U X F
da cui:
VFG (ml/min) = U x F / P
Questa formula permette, quindi, di calcolare la velocità di filtrazione glomerulare soltanto se la sostanza impiegata viene completamente filtrata, ma non riassorbita né secreta a livello tubulare e tutta escreta.
Non ci sono sostanze endogene nel nostro organismo che rispondono in maniera completa a queste caratteristiche. Dobbiamo, quindi, prendere in considerazione una sostanza esogena. La sostanza che di solito viene utilizzata a tal fine è l'inulina. Questa sostanza è un polimero del fruttosio; ha dimensioni molecolari (5.200 circa) tali da passare liberamente attraverso il filtro glomerulare, non è riassorbita in maniera significativa dai tubuli, né secreta. Di conseguenza, essa viene a trovarsi nel filtrato glomerulare alla stessa concentrazione che nel plasma arterioso e passando nei tubuli viene interamente eliminata nelle urine.
Si
supponga, per esempio, che la concentrazione di inulina del plasma sia pari a
0,1 g/100 ml e che
Perciò la velocità di filtrazione glomerulare nell'uomo è considerata pari a 125 ml/min.
FRAZIONE DI FILTRAZIONE
È la frazione del plasma passante attraverso i reni che viene filtrata. Poiché il flusso plasmatico normale efficace attraverso ambedue i reni (vedi clearance del PAI a pag.40) è di 650 ml/min e la normale VFG è di 125 ml/min, la frazione di filtrazione media (FF) risulta essere data dalla formula:
FF= Ci / CPAI = 125 / 650= 0,19
In condizioni basali, quindi, solo il 19% del plasma che passa attraverso i reni in un minuto viene filtrato.
Anatomia e fisiologia del rene Favaro S., Bordin V., Brunello A., Borsatti A. - Policlinico Universitario - Padova
Il rene svolge principalmente 4 funzioni:
ANATOMIA
MACROSCOPICA
I reni sono
localizzati in sede retroperitoneale, nella parete posteriore dell'addome, ai
lati della colonna dorso-lombare. Il polo superiore è a livello della 1/2
vertebra toracica, il polo inferiore raggiunge la 33 vertebra lombare. Il rene
dx è più basso di circa 1/2 vertebra per la presenza del fegato sul lato.
Medialmente al rene si trova l'ILO RENALE da dove passano vasi e nervi e vi
esce l'uretere. L'ilo immette nel SENO RENALE, cavità appiattita con vasi,
nervi, tessuto adiposo, circondato da parenchima renale; nell'ilo renale
l'uretere si espande per formare
ANATOMIA
MICROSCOPICA
In sezione sagittale nei reni si distinguono 2 porzioni:
Contiene:
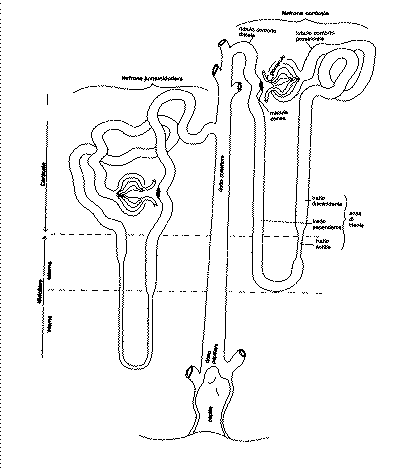
Quindi
NEFRONE = CORPUSCOLO RENALE + TUBULO
Esiste una duplice popolazione di nefroni:
CORPUSCOLO DI MALPIGHI = GLOMERULO (fitta rete di capillari) + CAPSULA DI BOWMANN
In ogni CORPUSCOLO si riconosce (Fig.2):
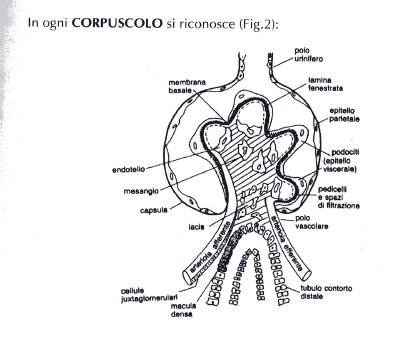
POLO VASCOLARE
(dove entra
l'arteriola afferente, si sfiocca nei capillari glomerulari ed esce l'arteriola
efferente). E' da rilevare che i rami derivanti dall'arteriola non hanno
connettivo cioè non esiste connettivo all'interno del glomerulo ma MESANGIO,
che è un tessuto di sostegno formato da cellule e matrice, che accompagna i
vasi sanguigni. Le cellule mesangiali posseggono numerosi filamenti di actina e
miosina ed hanno capacità contrattile come le cellule muscolari liscie,
permettendo la regolazione del circolo sanguigno nel glomerulo mediante
variazioni del lume vascolare. Hanno inoltre funzione macrofagica cioè
"ripuliscono" la membrana basale glomerulare e producono sostanze
immunoflogistiche che appartengono al gruppo delle prostaglandine, citochine e
fattori di crescita. 1/interazione fra queste sostanze gioca un ruolo
importante nella glomerulonefrite.
POLO URINARIO
diametralmente opposto al polo vascolare. Qui la capsula di Bowmann si
restringe in un tubulo che costituisce la seconda parte del nefrone.
è una struttura che si trova all'estremità cieca, dilatata del tubulo
urinifero; essa invagina il glomerulo. E' costituita da: un FOGLIETTO VISCERALE
aderente alle anse capillari. Questo si riflette sul FOGLIETTO PARIETALE che si
continua col tubulo prossimale. Il parietale è formato da cellule piatte, il viscerale
da podociti: sono cellule fornite di molti prolungamenti e da questi
prolungamenti derivano i pedicelli tramite i quali la cellula aderisce ai
capillari. I podociti hanno un rivestimento costituito da mucopolisaccaridi
ricchi di acido sialico; ciò rende la superficie carica negativamente e questa
condizione è necessaria per la permeabilità del filtro. Tra f. viscerale e f.
parietale c'è una fessura glomerulare dove arriva l'ultrafiltrato che passa nel
tubulo. Per quanto riguarda la formazione della preurina cioè l'ultrafiltrato
del plasma, sono importanti tré strutture:
Il filtro glomerulare funziona da setaccio e regola il passaggio delle macromolecole secondo le loro dimensioni e le loro cariche.
TUBULO
Si distingue
in:
COLLETTORE
II tubulo
contorto distale si innesta nel collettore. I collettori terminano nei dotti
papillari di Bellini che si affaccianno nelle papille renali.
APPARATO fUXTAGLOMERULARE (fig.3)
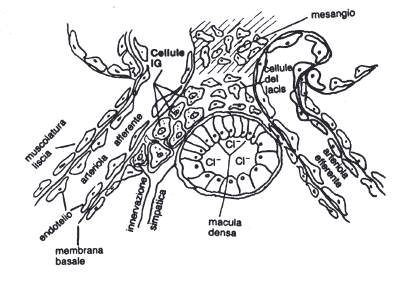
E' una struttura situata nel polo vascolare del corpuscolo. Comprende:
Cellule
juxtaglomerulari
Sono presenti
nella parete dell'arteriola afferente poco prima decentrata nel glomerulo. Sono
cellule muscolari modificate denominate cellule mioepiteliali in quanto
presentano i caratteri di entrambi i tipi cellulari. Secernono renina.
Cellule della
macula densa (M.D.)
Nel tubulo
distale, vicino al polo vascolare, c'è un disco più scuro che è dato dalla M.D.
Queste cellule sono scure perché i nuclei sono addensati e ravvicinati tra
loro.
Cellule
mesangiali extraglomerulare
Sono situate
nell'angolo fra le 2 arteriole in continuità col mesangio intraglomerulare.
Sono simili alle cellule intraglomerulari cioè sono cellule ramificate, tra
loro intrecciate, immerse in una matrice extracellulare. Le cellule della M.D.
percepiscono la concentrazione di sodio nel tubulo distale. Se la
concentrazione di sodio diminuisce, le cellule juxtaglomerulari vengono
stimolate a produrre renina e ciò comporta riassorbimento di Na e H20. Le
cellule ilari funzionano da mediatori fra M.D. e cellule juxtaglomerulari:
mediano la formazione di renina da parte delle cellule juxtaglomerulari.
INTERSTIZIO
RENALE
E' poco
rappresentato nella corticale, molto nella midollare. E' costituito da cellule
e matrice.
CELLULE CORTICALI: sono cellule
simil-fibroblasti che servono a produrre la matrice in cui si trovano cellule
simil-monociti (che si possono trasformare in macrofagi) e cellule
simil-linfociti.
CELLULE MIDOLLARI: sono cellule stellate,
ricche di prolungamenti, piene di gocce lipidiche (precursori ormonali?),
cellule simil-linfociti e cellule simil-periciti che accompagnano i vasi.
VASI E
CIRCOLAZIONE INTRARENALE (Fig. 4)
Tramite le
arterie renali i reni ricevono 1.000-1.200 ml di sangue/m' (circa il il 20%
della portata cardiaca). L'80-90% della portata renale ematica (PRE) circola
nella corticale, il rimanente nella midollare. Nella regolazione della PRE
intervengono:
NB: per il fenomeno dell^'autoregolazione emodinamica renale" il flusso renale può rimanere relativamente costante nonostante ampie variazioni della PA sistemica.
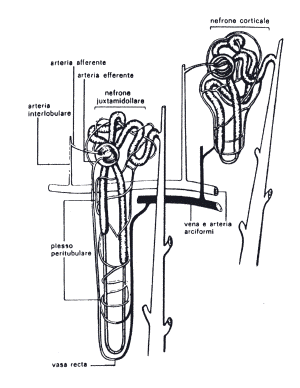
Nel parenchima renale l'Art. renale si divide nelle Art. interlobari le quali, livello della base delle piramidi si piegano ad angolo retto per decorrere ad arcata fra sostanza midollare e corticale (fig. 4); sono le cosiddette Art. arciformi dalle quali originano le Art. interlobulari che penetrano nella corticale in modo radiato; da queste ultime originano le Art. afferenti che penetrano nei glomeruli, si sfioccano in molti capillari che danno origine alle Art. efferenti. Le arteriole efferenti hanno un diverso andamento a seconda della posizione del glomerulo. Nel nefrone corticale l'Art. efferente termina in una fitta rete di capillari tubulari che irrorano i tubuli, alcune porzioni dell'ansa di Henle e dei collettori. Dai capillari venosi posti a tale livello inizia il circolo refluo renale:
vene interlobulari > vv. arciformi > vv. interlobari > v. renale > V. cava inferiore.
Nel nefrone juxtamidollare le arteriole efferenti vanno a formare una rete capillare peritubulare e, dirigendosi in bassonnelle piramidi, i vasa recta. Questi ultimi discendono nella midollare radialmente con decorso parallelo a quello dell'ansa di Henle, poi risalgono nella parte più esterna delle piramidi e si immettono in una vena arciforme o in una vena interlobare.I vasa recta, con la loro disposizione ad ansa sono importanti per mantenere il gradiente osmotico interstiziale corticomidollare che a sua volta è importante per il riassorbimento dell'acqua a livello dei collettori.
FORMAZIONE
DELL'URINA
II sangue
che, arrivando dall'arteria renale, passa attraverso i capillari glomerulari
viene ultrafiltrato dando origine ad un soluto simile a plasma ma molto povero
in proteine. Il filtro glomerulare permette il passaggio di acqua e soluti a
basso peso molecolare come ad esempio Na+, urea, inulina, mioglobina fino
all'albumina (PM| 69000 d.). Questo fa si che vengano trattenute, in base al
peso molecolare, molecole come le proteine mentre c'è un libero scambio di
acqua ed elettroliti. Per le proteine il meccanismo di filtrazione è regolato
oltre che dal peso molecolare e dalle loro dimensioni, anche dall'essere le
molecole proteiche cariche negativamente. Poiché anche nella membrana basale
glomerulare sono presenti cariche negative (dovute ai proteoglicani) si crea a
questo livello una repulsione elettrostatica che impedisce
l'ultrafiltrazione.Le forze che regolano la formazione dell'ultrafiltrato o FGR
sono (Fig.6):
Poiché anche il passaggio di liquido attraverso la membrana basale dei capillari glomerulari segue la legge di Starling, esso avviene secondo questa formula:
FGR=Lp.S(Pg-Pg)-(g-b)
dove:
Lp= coefficiente di
permeabilità attraverso il capillare glomerulare
S= superficie di filtrazione
Pg e Pb= pressione idrostatica nel capillare glomerulare e nella capsula di
Bowmann
g e b= pressione osmotica nel capillare glomerulare e nella capsula di Bowmann.
Poiché b è uguale a zero (non ci sono proteine nell'ultrafiltrato) il calcolo
del FGR sarà dato dalla formula:
FGR= Lp.S Pg- Pb)- b
CONTROLLO DELLA
FILTRAZIONE GLOMERULARE
La
filtrazione glomerulare è regolata da:
A.
sostanze vasoattive che circolano nel plasma o sono
prodotte dal rene. Ricordiamo tra le più importanti l'angiotensina II e la
noradrenalina vasocostrittrici, le prostaglandine vasodilatatrici. Vale la pena
a questo proposito ricordare che gli anti infiammatori non steroidei (aspirina,
indometacina) essendo inibitori della sintesi delle prostaglandine possono
ridurre il FGR causando una insufficienza renale acuta.Il rene possiede inoltre
una elevata capacità autoregolante per cui, variando le resistenze delle
arteriole afferente ed efferente, riesce a mantenere costante il flusso
plasmatico renale e quindi il FGR anche per ampie variazioni di pressione
arteriosa sistemica (da
B. Il sistema di feedback tubulo-glomemlare per cui se varia la pressione di perfusione glomerulare e quindi la concentrazione di soluti, soprattutto cloro e sodio, a livello della macula densa parte uno stimolo di vasocostrizione all'arteriola efferente che lo riporta alla norma.
C. Il bilancio glomerulo-tubulare che consiste in una correlazione funzionale tra i due elementi per cui il riassorbimento di acqua e soluti dipende da variazioni dell'FGR, tale correlazione fa si che nel tubulo prossimale il 60% dell'ultrafiltrato venga riassorbito quale che sia l'entità del filtrato stesso.
FUNZIONE
TUBULARE
Poiché
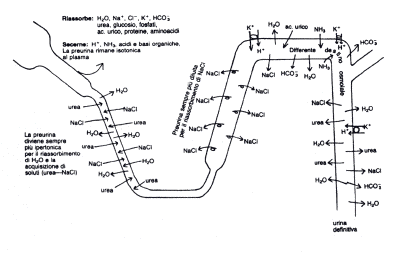
FUNZIONE DEL
TUBULO PROSSIMALE
II tubulo
contorto prossimale per la presenza di numerose introflessioni (Fig. 8) della
membrana cellulare sia nella superficie basale che luminale offre una grande
possibilità di contatto per la preurina che vi arriva; essendo inoltre le sue
cellule ricche di enzimi riesce, oltre che a riassorbire, a lavorare attivamente
elaborando ciò che riassorbe. A questo livello il fluido rimane isoosmotico col
plasma, ma riassorbe quasi completamente glucosio, acido urico, aminoacidi e
bicarbonati. Acqua e sodio vengono riassorbiti per il 65% con modalità
"attiva" per il Na "passiva" per l'acqua. Per il
riassorbimento e/o la secrezione di altre sostanze invece la limitante è data
dalla Tm (tubular mass). Questo termine indica il limite critico sia di
riassorbimento che di secrezione, oltre al quale il tubulo non
"lavora" più. Ad esempio tutto il glucosio filtrato viene riassorbito
se la glicemia rimane nei limiti di norma, se invece vi è iperglicemia aumenta
il carico filtrato e aumenta la quantità riassorbita. Quando l'iperglicemia
supera valori di 180mg% il tubulo esaurisce la sua capacità di adattamento e
compare glicosuria. 1 80mg % di glicemia determina così la soglia renale per il
glucosio. Superato il tubulo prossimale la preurina, ancora isoosmotica e pari
al 20-30% dell'ultra filtrato entra nell'ansa di Henle. Oltre a queste funzioni
di rassorbimento il tubulo prossimale ha anche funzioni secretorie che portano
all'immissione nel fluido tubulare di ioni H+, cationi e anioni organici.
ANSA DI HENLE
L'ansa di
Henle (fig. 5) è formata da un tratto discendente permeabile solo all'acqua
mentre il tratto ascendente è permeabile al sodio e al doro (non all'acqua).
CONCENTRAZIONE
E DILUIZIONE DELL'URINA
Come si può
vedere nella figura n° 5 il liquido isosmotico che arriva dal tubulo prossimale
subisce un rimaneggiamento che, in collaborazione tra tratto discendente e
ascendente dell'ansa di Henle, tubulo distale, collettore e vasa recta, porta a
delle variazioni di concentrazione dei soluti e quindi della osmolarità
urinaria. Nell'ansa di Henle si ha un riassorbimento attivo (Na+K+ATPasi
dipendente) del 15-20% del Na+CI- filtrato. Questo avviene soprattutto nella
parte ascendente dell'ansa stessa dove si ha anche riassorbimento dei
bicarbonati filtrati, derivanti dal tubulo prossimale e del calcio sotto
controllo del PTH. Il meccanismo di concentrazione-diluizione si ha attraverso
il cosiddetto "meccanismo controcorrente. Il principio su cui si basa tale
fenomento, è rappre¬ sentato da:
I' iperosmolarità della
midollare a sua volta è regolata dal flusso continuo dei vasa recta che rimuove
i soluti. Quindi, per riassumere, l'urina isoosmotica del tubulo prossimale
diventa iperosmotica nella branca discendente, ipoosmotica nell'ascendente e
raggiunge l'osmolarità finale nel collettore per effetto dell'ADH. Il
meccanismo di concentrazione controcorrente permette variazioni di osmolarità
urinaria che vanno da
TUBULO DISTALE
II tubulo distale che inizia con la macula densa, è la sede in cui viene
riassorbito circa il 5% dell'NaCI. L'energia è data da una pompa Na+K-ATPasi,
localizzata nella membrana basolaterale delle cellule tubulari. Tale
riassorbimento è correlato solo con la quantità di Na+ che arriva dal tubulo
prossimale e quindi partecipa al mantenimento del bilancio glomerulo-tubulare;
non è infatti influenzato da ormoni come l'aldosterone, ma solo dalla
concentrazione di Na+ nel liquido tubulare. Poiché la concentrazione di Na+ che
arriva al tubulo distale è pari a 75mEq/L, a riassorbimento avvenuto essa sarà
pari a 40 mEq/L. Nel tubulo distale avviene anche un processo di secrezione
attiva di Ca++ mediata dal PTH, dal Calcitriolo e da una pompa
Ca++ATPasi.
TUBULO
COLLETTORE CORTICALE
II tubulo collettore corticale è formato da 2 tipi di cellule:
Le cellule principali presentano canali per Na+ e K+ e una pompa Na+K+ATPasi sulla membrana basolaterale. Attraverso questi canali vi è un riassorbimento attivo di Na+ che, creando una differenza di potenziale permette il riassorbimento passivo di CI- e la secrezione di K+ nel lume tubulare. In tale attività vi è una chiara funzione dell'aldosterone tesa ad incrementare il riassorbimento di Na+ e la perdita di K+. Un ulteriore funzione di questo segmento di nefrone è il riassorbimento delll'acqua ADH dipendente. Le cellule interposte invece regolano l'equilibrio acido-base: infatti in presenza di anidrasi carbonica, acqua e diossido di carbonio, formano H+ e HC03-. Successivamente l'HC03- in scambio con il CI- viene riassorbito in circolo attraverso la parete del lato basale delle cellule mentre lo ione H+ viene escreto nel lume tubulare tramite una pompa ATPasi dipendente. Tale pompa è, a sua volta attivata dall'aldosterone e questo spiega perché nell'iperaldosteronismo vi sia un aumento dell'escrezione di H+.
COLLETTORE
MIDOLLARE
In questo segmento del nefrone si ha la modificazione finale dell'urina. Il
tubulo infatti può riassorbire Na+CI- in quantità tali per cui, in caso di
bisogno, la concentrazione urinaria di Na+CI- si può ridurre a meno di 1mEq/L.
Per effetto dell'adiuretina il tubulo collettore midollare può riassorbire
ancora acqua ed urea permettendo così grosse variazioni dell'osmolarità
urinaria. Infine attraverso una pompa H+ e K+ ATPasi dipendente può secernere
attivamente H+ e riassorbire K+. Tali funzioni sono dipendenti dai tassi
plasmatici di aldosterone e dal pH ematico.
IL RENE COME
ORGANO ENDOCRINO
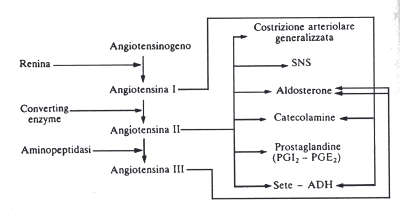
SISTEMA RENINA-ANGIOTENSINA
II sistema è raffigurato nella Fig. 6. Per quanto concerne le sedi di
produzione è da dire che la renina (un enzima proteolitico di PM 40.000) è
localizzato nei granuli delle cellule dell'apparato juxtaglomerulare mentre il
suo substrato, l'angiotensinogeno, è una glicoproteina di origine epatica. Gli
stimoli per la sua dismissione sono di tipo barocettore (pressione transmurale
dell'arteriola afferente) e chemocettore (contenuto in Na+Ci- a livello della
macula densa). Esiste anche una produzione di renina mediata dall'attività
nervosa simpatica, dalla concentrazione di prostaglandine, paratormone,
istamina, ADH ed infine dalla concentrazione plasmatica di K+ e di AT II.
Fondamentalmente il sistema ha un'azione proipertensiva attraverso 3
meccanismi:
A. effetto vasocostrittore per azione diretta della AT II sulle miocellule della parete| vascolare (lo stimolo più efficace è una brusca riduzione della volemia);
B. stimolo alla produzione surrenalica dell'aldosterone con aumento del riassorbìmento di Na+ a livello dei tubuli collettori;
C. stimolo diretto dell'AT II sul tubulo prossimale con conseguente riassorbimento tubulare di Na+. Inibitori del sistema sono i tarmaci bloccanti, tutto ciò che inibisce la produzione di catecolamine e, di ampio uso terapeutico, gli inibitori del convertyng M enzyme che inibiscono la trasformazione dell' AT I in AT II.
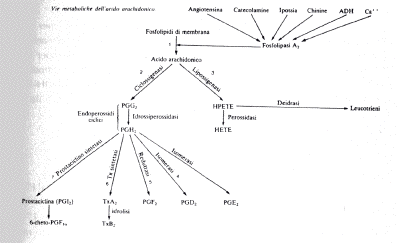
PROSTAGLANDINE
La produzione
delle prostaglandine dai fosfolipidi di membrana è rappresenta¬ ta nella fig.
7. Nella tabella è indicato il loro effetto finale e il bersaglio della loro
azione è rappresentato dalle arteriole glomerulari, dai tubuli (soprattutto
collettore) e dal mesangio. La loro sintesi è inibita soprattutto da tarmaci
anti-infiammatori non steroidei per effetto diretto sull'enzima
cicloossigenasi.
ERITROPOIETINA
E' un ormone prodotto dal rene di natura polipeptidica di PM 34.000. La sede di
produzione non è nota: forse nella midollare, forse a livello dell'apparato
juxta-glomerulare. L'ormone stimola l'eritropoiesi con i seguenti meccanismi
(fig):
A. induce la maturazione e la trasformazione delle cellule midollari in eritrociti;
B. stimola la sintesi di emoglobina;
C. stimola la immissione in circolo di reticolociti.
La sua produzione è indotta da tutto ciò che diminuisce la produzione renale di ossigeno come la riduzione del flusso o anemia. E' stimolato anche da corticco steroidi, ACTH, ormoni tiroidei e testosterone.
CALLICREINE E
CHININE
Le
callicreine sono proteasi che portano alla formazione di chinine da un
substrato plasmatico: il chininogeno. La produzione renale (ne esiste anche una
plasmatica) di chinine è stimolata dai mineralcorticoidi e non ha effetti extrarenali.
La loro azione a livello renale provoca un aumento del flusso, della diuresi e
della escrezione di Na.
VITAMINA D
Il rene
interviene nella regolazione del metabolismo dell'osso sia per azione diretta
sul bilancio calcio-fosforo sia producendo il metabolita attivo della viamina
D.
Gli stimoli alla produzione sono rappresentati dalla ipofosforemia e dal PTH. La funzione endocrina finora descritta è peculiare del rene normale. E' però utile sottolineare che è di recente acquisizione la conoscenza che il tessuto renale sotto stimolo patogeno (ischemico, tossico, infettivo, immuno-allergico) diventa sede di produzione di sostanze ad azione ormono-simile che interferiscono ne! sistema di coagulazione dei processi infiammatori acuti e cronici e immunologie. La produzione di tali sostanze avviene a livello mesangiale, epiteliale ed endoteliale. Esse sono rappresentate fondalmentalmente da citochine:
La produzione di tali sostanze è inoltre aumentata anche per l'arrivo di cellule circolanti come macrofagi, T linfociti e polimorfonucleati al tessuto renale richiamati dalla lesione in atto. Il bersaglio di tali sostanze autocrino e paracrino è rappresentato a sua volta dalle stesse strutture parenchimali renali (glomeruli, interstizio, vasi) la cui risposta può essere di difesa e quindi di risoluzione del processo patologico in atto o di aggravamento e di autoperpetuarsi di un meccanismo lesivo (vedi patologia autoimmune).
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2025