|
|
| |
 Università degli Studi di Trieste
Università degli Studi di Trieste
FACOLTA' DI INGEGNERIA - LABORATORIO DI FISICA
Determinazione indiretta del calore specifico di un solido mediante l'uso di un calorimetro adiabatico delle mescolanze. 222b14c

Data: Allievo: Cappelli Alessandro Visto:___________
In figura è rappresentato il calorimetro delle mescolanze, chiamato anche calorimetro di Reneult. Esso essenzialmente è costituito di un contenitore costruito in modo tale da permettere perdite di calore molto piccole e quindi trascurabili, cioè è reso adiabatico. All'interno è contenuta un certo volume d'acqua nel quale a sua volta è completamente immerso un corpo di metallo.
Il coperchio del calorimetro è dotato di fessure a misura per permettere l'inserimento di un agitatore e un termometro. L'agitatore è necessario per la rapida e uniforme distribuzione della temperatura. In questa prova è stato utilizzato un termometro digitale.
E' stato adottato l'uso di un termometro digitale in quanto in questa prova è necessario rilevare istantaneamente il variare delle temperature. L'utilizzo di un termometro analogico comprometterebbe i risultato dell'esperimento in quanto il tempo di reazione dello strumento è troppo grande. La sensibilità dello strumento da noi utilizzato è 0,1°C.
Cronometro digitale
Nuovamente è stato necessario l'uso di uno strumento di precisione: un cronometro digitale. Infatti questo ha permesso di scandire in modo preciso gli intervalli di rilevazione della temperatura. La sua sensibilità è pari a 0,01 sec.
Lo scopo dell'esperienza è quello di individuare, mediante calcoli da dati ricavati sperimentalmente, il calore specifico del corpo solido preso in considerazione.
Il calore specifico per definizione è la quantità di calore necessaria per far aumentare di 1°C la temperatura di una determinata massa unitaria. Per giungere a questo fine è stato quindi utilizzato il calorimetro delle mescolanze; esso è stato riempito di acqua a temperatura ambiente ed in essa è stato immerso il corpo solido del quale si doveva calcolare il calore specifico. Il corpo però è stato immerso ad una temperatura superiore a quella dell'acqua. Trascorso un certo intervallo di tempo il sistema acqua-corpo solido ha raggiunto una temperatura di equilibrio. Analiticamente quindi si può scrivere:
![]()
dove QA è il calore scambiato dall'acqua mentre QC è il calore scambiato dal corpo solido. Ricordando che in generale Q = c m (t2 - t1), l'espressione precedente diventa:
![]()
dove C rappresenta la capacità termica del calorimetro, nota. In conclusione il calore specifico del corpo in questione è dato da:
A ![]()
dove m' rappresenta l'equivalente in acqua del calorimetro.
Massa dell'acqua m = 150 g Dm = 2 g
Equivalente in acqua m' = 15 g Dm = 4 g
Massa del corpo M = 25,000 g DM / M = 0,1% Dm = 0,025 g
Temperatura dell'acqua t = 25,4°C Dt = 0,1°C
Temperatura del corpo T = 99,6°C Dt = 0,1°C
Temperatura di equilibrio te = 27,9°C Dt = 0,1°C
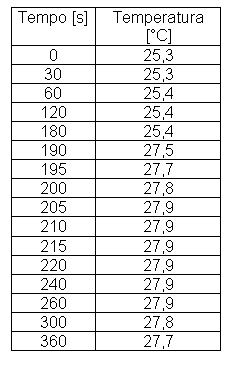
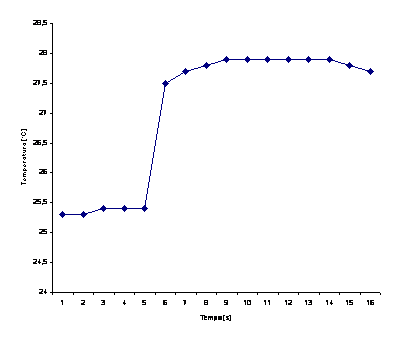
Una volta immerso il corpo caldo nell'acqua e chiuso il coperchio del calorimetro si effettuano le rilevazioni delle temperature a distanza di intervalli uguali di tempo. In questo modo è possibile ricavare un grafico temperatura / tempo.
Dalla formula A si può ricava cx = 0,23 [cal g-1 °C-1]
La misura è indiretta e non ripetuta, quindi per il calcolo dell'errore si utilizza la seguente:
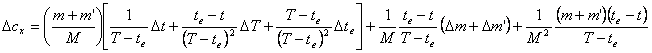
![]()
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2025