|
|
| |
Corso di laurea in Biotecnologie
Esame di Laboratorio di Chimica Biorganica
Scopo di questa esercitazione è la sintesi di un dipeptide, l'aspartilfenilalanina, la sua purificazione e successivamente l'analisi dello spettro NMR. Si sono sciolti 50mg 858d38i di BOC-Asp-OtBu in 1ml di CH2Cl2 anidro in un pallone e si sono aggiunti 80mg di DCC. Il pallone, tappato, è stato lasciato in agitazione per 15 minuti.
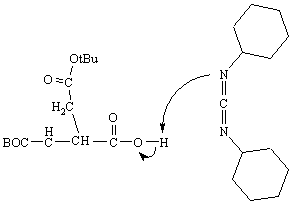
L'asp utilizzato ha il gruppo carbossilico della catena laterale esterificato da t-Butanolo e porta legato al gruppo amminico il BOC, in modo da evitare reazioni non desiderate. Il gruppo carbossilico legato al Ca è l'unico libero di reagire.
![]()
La DCCI viene aggiunta per attivare il gruppo COOH e renderlo più
suscettibile all'attacco nucleofilo da parte del gruppo
-NH2 della fenilalanina.
![]()
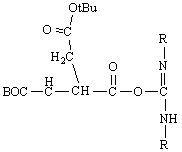

In un altro pallone si sono contemporaneamente sciolti 50mg di Phe-OMe · HCl in 1ml di CH2Cl2 anidro a cui si sono aggiunti 40ml di DIEA. Il pallone, tappato, è stato lasciato sotto agitazione per qualche minuto.
La fenilalanina, diversamente dall'aspartilfenilalanina, ha il gruppo amminico libero di reagire mentre il gruppo COOH è protetto come estere metilico.
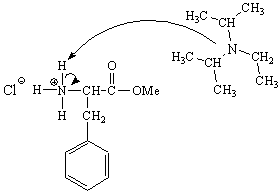
![]() La fenilalanina è però presente come sale di HCl e
l'aggiunta di DIEA è necessaria per deprotonare il gruppo NH3+ e
renderlo libero di reagire con il gruppo carbonilico attivato dell'Asp.
La fenilalanina è però presente come sale di HCl e
l'aggiunta di DIEA è necessaria per deprotonare il gruppo NH3+ e
renderlo libero di reagire con il gruppo carbonilico attivato dell'Asp.
La DIEA quindi forma il suo sale con HCl.
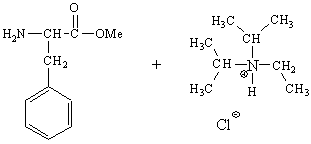
La Phe è stata aggiunta all'Asp con una pipetta Pasteur, pulita e asciutta, e la miscela è stata lasciata a reagire nel pallone, tappato, sotto agitazione e a temperatura ambiente, per circa 1h.
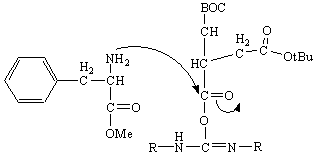
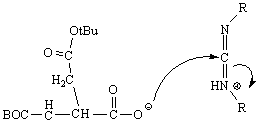
Il gruppo -NH2 della Phe attacca il carbonile attivato dell'Asp, con la formazione del dipeptide e DCU.
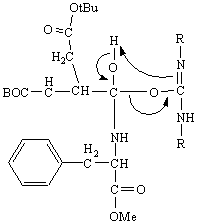
![]()
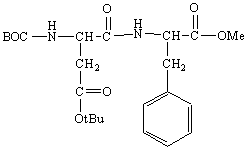
![]()
Terminata la reazione si è eseguita una TLC di silice, usando come eluente CHCl3 : Acetato di etile (98:2).
La cromatografia si esegue per confrontare gli Rf dei due reagenti con quello della miscela di reazione, in modo da valutare se la reazione ha avuto luogo o no.
Evidenziata dalla TLC l'avvenuta reazione, la soluzione è stata trasferita in un altro pallone utilizzando una pipetta Pasteur con dell'ovatta all'estremità per effettuare un filtraggio che consente di eliminare le impurità più grosse, come i cristalli di DCU.
La soluzione così filtrata è stata seccata alla pompa. Si è poi proceduto alla purificazione del dipeptide.
La miscela di reazione è stata sciolta nella minore quantità di cloroformio possibile. È stata poi preparata una lastra di gel di silice, sulla quale, in più riprese, è stata caricata tutta la miscela di reazione.
Non è stato necessario compattare il campione facendolo migrare per qualche cm in etere etilico, in quanto il caricamento è stato ben eseguito.
Il campione così preparato è stato fatto migrare nella miscela di eluizione CHCl3 : Acetato di etile (9:1) finché non è arrivato ad un paio di cm dal bordo della lastra.
La cromatografia è stata eseguita per poter separare le diverse componenti della miscela di reazione, che oltre al dipeptide, contiene anche altri composti che non interessano.
Si conosceva già in precedenza quale fosse la banda contenente il dipeptide; in caso contrario sarebbe stato necessario effettuare una NMR su tutte le diverse componenti della miscela per individuare la banda del dipeptide neosintetizzato.
La lastra è stata asciugata, si è grattata mediante una spatola la banda da analizzare ed è stata presa anche la tara di un pallone di 100 cc.
Si è così separato dal resto la silice a cui si trova legato il dipeptide.
La silice è stata poi caricata su un gooch e, mediante una pompa a vuoto, è stata eluita con cloroformio e portata a secco nel pallone.
In questo modo si è separato il dipeptide dalla silice.
L'operazione è stata ripetuta più volte, fino a peso costante del pallone, ottenendo così la certezza di aver recuperato la maggior quantità possibile del dipeptide.
Su questo campione si è infine eseguita una NMR. I risultati ottenuti concordano con quelli previsti.
Il composto sintetizzato è quindi realmente la aspartilfenilalanina.
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2025