|
|
| |
TITOLO: Saggi di riconoscimento alla fiamma
OBIETTIVO: Mediante l'osservazione delle colorazioni che assume la fiamma mentre ossida un composto del quale conosciamo unicamente la formula chimica, identificare l'elemento che lo compone.
MATERIALI/STRUMENTI: Becco Bunsen; 5 Vetrini; Ansa munita di filo di Nichel-Cromo; Becher contenente acido 515b15f cloridrico; 5 Provette dotate di tappo contenenti: Cloruro di Litio (LiCl), Cloruro di Potassio (KCl), Cloruro di Sodio (NaCl), Cloruro di Stronzio (SrCl) e Solfato di Rame (CuSO4).

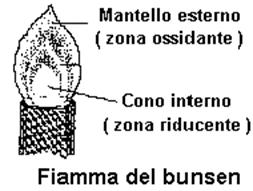
Figura 1: Becco Bunsen

Figura 2: Cloruro di Litio

Figura 3: Cloruro di Potassio

Figura 4: Cloruro di Sodio

Figura 5: Cloruro di Stronzio

Figura 6: Solfato di Rame

Figura 7: Acido Cloridrico
PROCEDIMENTO:
Accendere il bunsen
Immergere il filo di Ni-Cr nell'acido cloridrico e poi posizionarlo sulla fiamma per pulirlo da eventuali residui di una qualche sostanza.
Con l'ansa prelevare piccole quantità di un cloruro o del solfato (inserendola nelle provette stappate) per poi posizionare il filo sulla parte più calda della fiamma.
Ripetere il procedimento descritto nel punto 2 e poi quello del punto 3 per ogni sostanza, osservando ogni volta la colorazione assunta dalla fiamma.
RACCOLTA DATI/RISULTATI:
|
Sostanza analizzata |
Colore assunto dalla fiamma |
|
Cloruro di Litio |
Rosso cardinale (ciliegia) |
|
Cloruro di Potassio |
Viola* |
|
Cloruro di Sodio |
Giallo intenso |
|
Cloruro di Stronzio |
Rosso acceso (a sprazzi) |
|
Solfato di Rame |
Verde |
*meno visibile a causa dell'elevata volatilità.



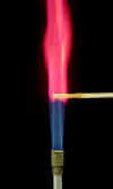

Le varie colorazioni assunte dalla fiamma a seconda della sostanza riscaldata (nelle immagini, dal LiCl al CuSO4)
CONCLUSIONI: Attraverso la colorazione che la fiamma ha assunto, ogni volta differente a seconda del metallo presente nei composti*, è stato possibile raggiungere l'obiettivo e classificare le varie sostanze.
* quando ad un atomo si fornisce energia i suoi elettroni "saltano su livelli energetici più esterni, terminata l'eccitazione, essi tornano allo stato fondamentale, restituendo l'energia acquistata sotto forma di radiazione elettromagnetica. Poiché atomi di elementi diversi possiedono una differente struttura elettronica, emettono diverse radiazioni luminose e quindi luce di colore differente.
PROBLEMI/DIFFICOLTÀ: Non sono presenti particolari difficoltà, bisogna unicamente stare attenti a pulire bene il filo di Nichel-Cromo nell'acido cloridrico e poi nella fiamma per evitare contaminazioni di colore.
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2025