|
|
| |
Gli ATOMI
Tutta la materia è costituita da atomi (particelle infinitamente piccole costituite da particelle subatomiche ancora più piccole).
In natura, fino ad ora, sono stati scoperti 92 tipi di atomi e altri 20 sono stati creati in laboratorio; tutti questi tipi di atomi se si combinano tra di loro danno origine a tutte le sostanze esistenti sulla terra.
Le sostanze vengono quindi suddivise in sostanze semplici (sono le sostanze composte d 131j98b a uno o più atomi dello stesso tipo) o in sostanze composte (sono le sostanze composte da atomi di tipo diverso).
I composti chimici vengono identificati con una formula chimica che indica gli elementi che costituiscono il composto e le proporzioni a cui questi si combinano.
Ad esempio il glucosio (C6H12O6) è formato da 6 atomi di carbonio(C), 12 atomi di idrogeno (H) e da 6 atomi di ossigeno (O).
L'atomo è costituito da un nucleo contenente due tipi di particelle subatomiche:protoni con carica positiva (+) e neutroni con carica neutra e da degli orbitali esterni dove vi ruotano gli elettroni che posseggono una carica negativa(-).
Un atomo si differenzia da un altro attraverso il suo numero atomico e attraverso il suo numero di massa:
a
= n. di massa = massa protoni + massa neutroni
aHz
z = n. atomico = n. di protoni
H = lettera per identificare l'elemento
Secondo il modello atomico planetario gli elettroni sono disposti sugli orbitali con una disposizione ben precisa: tutti gli orbitali possono contenere un massimo di 8 elettroni tranne il primo (quello più vicino al nucleo) che ne può contenere un massimo di due; gli elettroni devono prima riempire completamente gli orbitali più interni per passare poi a quelli più esterni. Questa disposizione di elettroni si chiama configurazione elettronica dell'atomo.
I composti chimici si formano con l'unione di due o più atomi; questa unione si chiama legame.
I legami chimici si tendono a formare perché gli atomi tendono a raggiungere una configurazione stabile; quindi si può dire che i legami chimici vengono creati grazie alla condivisione o al trasferimento di due o più atomi.
Esistono due tipi di legami chimici: legami ionici e legami covalenti.
Nel legame ionico gli atomi "perdono" o "acquistano" un elettrone diventando così ioni; gli ioni sono atomi elettricamente carichi perciò gli atomi che hanno "perso" un elettrone diventano ioni positivi (+), e quelli che lo hanno "acquistato" diventano ioni negativi (-).
Siccome atomi di carica opposta si attraggono i due o più ioni si legano formando così un legame ionico.
Un esempio di legame ionico è il cloruro di sodio(NaCl), infatti il sodio possiede solo un elettrone nell'ultimo orbitale e dove nel cloro ne manca solo uno. Quindi il sodio cede l'atomo a cloro diventando ioni (sodio Na+ e il cloro Cl-); dopodiché si attraggono formando il comune sale da cucina.
Nel legame covalente non c'è una "perdita" o un "acquisto" di elettroni ma una condivisione di quelli sull'orbitale più esterno. Più elettroni si condividono più è forte il legame; si dice legame semplice quando ne condividono 2 elettroni, doppio legame quando ne hanno in comune 4 e triplo legame quando ne hanno 6 in comune.
Ad esempio: due atomi di ossigeno hanno sull'ultimo orbitale 6 elettroni quindi per raggiungere la stabilita condividono due elettroni ciascuno, formando così una molecola di ossigeno (O2).
La molecola dell'acqua (H2O) ha una leggera carica positiva ad una estremida e una leggera carica negativa nell'altra. Tutte le molecole che presentano questa situazione sono dette polari, e al contrario le altre sono dette non polari o apolari.
L'acqua ha la propieta di dissociarsi in due ioni H2O g H+ + OH-; questi due ioni hanno molta facilità a legarsi con sostanze diverse per creare composti diversi.
I composti che in soluzione producono ioni H+ sono chiamati acidi.
I composti che in soluzione producono ioni OH- sono chiamati basi.
Per indicare la maggiore o la minore presenza di ioni H+ o OH- si utilizza la scala del pH dove:
Le soluzioni con il pH < 7 sono dette soluzioni acide;
Le soluzioni con il pH > 7 sono dette soluzioni basiche;
Le soluzioni con il pH = 7 sono dette soluzioni neutre.
I composti si differenziano in composti organici e composti inorganici.
Quelli organici sono caratterizzati dalla presenza di almeno due atomi di carbonio (C) e almeno uno di: ossigeno (O), azoto (N), fosforo (P) o idrogeno (H).
La maggior parte della molecole organiche complesse sono polimeri (lunghe catene di molecole formate dall'unione di singole molecole più piccole chiamate monomeri).
Alcuni polimeri sono così grossi che vengono chiamati macromolecole; le principali macromolecole sono: i carboidrati, i lipidi, le proteine e gli acidi nucleici.
I carboidrati o glucidi sono formati da atomi di carbonio, ossigeno e idrogeno.
Di questa classe fanno parte gli zuccheri e gli amidi.
I carboidrati più piccoli sono chiamati monosaccaridi; che comprendono il galattosio, il fruttosio e il glucosio. Questi zuccheri semplici hanno la formula C6H12O6 ma differiscono tra loro nella struttura molecolare. Gli zuccheri vengono molto utilizzati dalle cellule per produrre energia chimica per questo le cellule riescono anche a costruire ed immagazzinare questi zuccheri semplici.
I carboidrati che si formano dall'unione di due monosaccaridi si chiamano disaccaridi (ad esempio il saccarosio), e quelli formati da più di due monosaccaridi vengono chiamati polisaccaridi (ad esempio l'amido e il glicogeno).
I LIPIDI
I lipidi comprendono: le cere, i grassi e i composti oleosi; possono essere utilizzati dagli organismi viventi per immagazzinare e produrre energia (come i carboidrati) ; inoltre essi costituiscono uno strato semipermeabile che riveste le cellule.
Sono formati da atomi di carbonio, idrogenno ed ossigeno.
Le molecole di lipidi possono avere forme assai diverse: gli acidi grassi sono lunghe catene di atomi di carbonio e di idrogeno alla quale è legato un gruppo carbossilico (COOH); il glicerolo è un alcol che ha tre atomi di carbonio che contengono tre gruppi ossidrilici (OH); altri lipidi, come il colesterolo, sono costituiti, invece, da una serie di anelli di atomi di carbonio uniti tra loro.
LE PROTEINE
Le proteine o protidi sono i componenti organici più presenti nel mondo vivente. Essi sono costituiti da atomi di carbonio, idrogeno, ossigeno e azoto.
Le proteine sono formate dall'unione di due o più amminoacidi.
Gli amminoacidi sono formati da una struttura generale: un atomo di carbonio lega con un atomo di idrogeno, con un gruppo carbossilico, con un gruppo amminico e con una variabile che differenzia i 20 amminoacidi. Legando un gruppo carbossilico di un amminoacido con il gruppo amminico dell'altro si crea una proteina formando dell'acqua; questa reazione è chiamata legame peptidico.
Se si legano 2 amminoacidi la proteina si chiamerà dipeptide, se gli amminoacidi sono da 3 a 10 si chiamerà oligopeptide e se gli amminoacidi sono più di 10 le proteine si chiameranno polipeptidi.
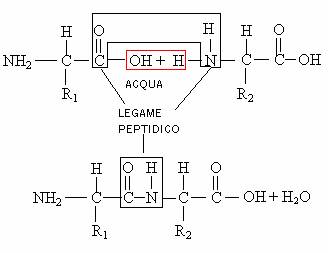 NH2 = gruppo amminico
NH2 = gruppo amminico
COOH = gruppo carbossilico
H2O = acqua
R1 - R2 = variabili
Esistono 20 tipi di amminoacidi che formano numerosi tipi di proteine
GLI ACIDI NUCLEICI
Gli acidi nucleici sono macromolecole formate da atomi di carbonio, idrogeno, ossigeno, azoto e fosforo. Servono a contenere le informazioni necessarie per il corretto funzionamento dell'organismo. Queste informazioni si chiamano caratteri ereditari e si tramandano dai genitori ai figli.
Gli acidi nucleici sono polimeri costituiti da monomeri chiamati nucleotidi e ogni nucleotide si può dividere in tre parti: gruppo fosfato, uno zucchero (può essere ribosio o dessiribosio; nel primo caso l'acido nucleico è il DNA o acido desossiribonucleico, nel secondo è l'RNA o acido ribonucleico) e da una base azotata.
Sia il DNA che l'RNA sono composti da quattro tipi di nucleotidi che si differenziano nella base azotata da essi contenuta: il DNA contiene Adenina (A), Guanina (G), Timida (T) e Citosina (C); l'RNA, invece, contiene le stesse basi azotate del DNA solo cha al posto della Timida c'è l'Uracile (U).
Il DNA ha una struttura molto complessa chiamata "a doppia elica", infatti essa è formata da due filamenti di nucleotidi che si collegano tra loro grazie alle loro basi azotate.
L'RNA, invece, è formata da una sigola catena di nucleotidi.
All'interno della cellula queste macromolecole servono per trasmettere le informazioni.
Gli enzimi sono proteine che servono a regolare ed ad agevolare delle reazioni chimiche (processo in cui si trasformano delle sostanze di partenza chiamate reagenti in un altro insieme di sostanze chiamate prodotti).
Gli enzimi agiscono come catalizzatori (sostanze che accelerano le reazioni chimiche e che rimangono intatti al termine di esse) perché accelerano le reazioni riducendo al minimo la quantita di energia utilizzata.
La reazione avviene facendo legare i substrati (reagenti) in dei siti attivi posizionati sugli enzimi così da far avvenire subito la reazione. Ogni enzima può catalizzare uno ed un solo tipo di reazione chimica, infatti i siti attivi si adattano ad un solo tipo di substrato. Quando i prodotti può ospitare altri substrati e ripetere tutto il processo.
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2025