|
|
| |
Corrente di sodio persistente (INaL)
La corrente di sodio nel miocardio è stata caratterizzata e suddivisa in due componenti principali: la componente transiente (INaT), condizionata dalla veloce cinetica di attivazione e inattivazione del canale, e la componente persistente, di ampiezza molto minore, ma presente durante tutta la fase di plateau (fase 2) del potenziale d'azione 51
La natura della corrente di sodio persistente può originare da due possibili meccanismi: la corrente "di finestra" e la corrente "tardiva" (INaL). La corrente di finestra è presente in uno stretto range di potenziali di membrana nel quale, anche allo stato stazionario, c'è parziale attivazione e incompleta inattivazione dei canali. Quando il potenziale di membrana raggiunge la "finestra" durante la ripolarizzazione, una frazione di canali recupera dall'inattivazione e si riattiva, permettendo un flusso di ioni 52;53. Durante una misura in condizioni di Voltage-Clamp, in cui il potenziale è manten 353d38d uto costante, le correnti di finestra mostrano la propria natura di fenomeni tempo-indipendenti: nel range di potenziale corretto infatti è sempre presente una frazione di canali che recuperano dall'inattivazione e conducono corrente. Tuttavia la sovrapposizione delle curve di attivazione e inattivazione dei canali ionici del sodio è abbastanza ristretta e, nei miociti ventricolari, tale sovrapposizione avviene in una regione di potenziali normalmente più negativi rispetto a quello della fase di plateau del potenziale d'azione: ne consegue che la corrente di finestra principalmente coinvolta nella fase 2 è quella di calcio, mediata dai canali di tipo L. (ICaL)54;55;55;56
La corrente INaL invece è un flusso ionico che si può misurare in potenziali al di fuori del range di finestra ed è presente normalmente in numerosi tipologie di miociti cardiaci (atriali, ventricolari o fibre del Purkinje).57-59 INaL può essere misurata anche in sistemi di espressione eterologa dei canali del sodio NaV 1.5, ovvero l'isoforma maggiormente presente nel miocardio, suggerendo che INaL sfrutta la stessa entità molecolare coinvolta nella INaT.54 La INaL corrisponde ad una riapertura di canali precedentemente inattivati nonostante il persistere della depolarizzazione; tale attività si presenta con differenti modalità di gating, definite "burst opening" e "scattered late opening". (Fig. 1.5)
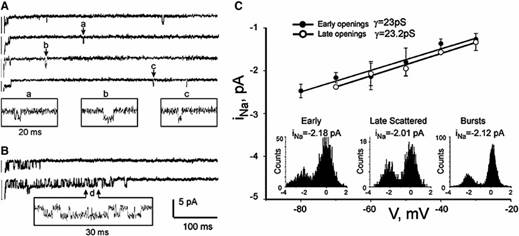
Fig. 1.5 Esempi di registrazione a singolo canale durante uno step di depolarizzazione attivante; il pannello A mostra l'iniziale breve apertura (tipiche della modalità di gating "early", che è correlato a INaT) e le seguenti aperture brevi tipiche del gating "scattered late", mentre il pannello B mostra aperture sostenute, tipiche della modalità di gating "burst". Il pannello C mostra le relazioni corrente-voltaggio e gli istogrammi di ampiezza della corrente registrata: come si può osservare le tre tipologie di apertura hanno la stessa conduttanza unitari; questo suggerisce che i tre fenomeni rappresentano differenti modalità di gating dello stesso canale.
Nel "burst mode" il canale ha una serie di aperture ripetute e di lunga durata; tali aperture permettono l'ingresso di una corrente a lenta inattivazione, di ampiezza molto inferiore a quella della INaT. Nelle aperture di tipo "scattered" invece il canale si riapre sporadicamente con una durata di apertura breve, simile a quelle della INaT, ma la corrente che ne deriva non mostra inattivazione. La INaL è definibile dunque come il risultato di "instabilità" dello stato inattivato, che consente ai canali di tornare conduttivi per brevi periodi di tempo.54
Normalmente, nei miociti ventricolari la INaL ha un'ampiezza inferiore all'1% della INa di picco (INaT), ma numerosi fattori possono provocarne l'aumento; alcuni di questi fattori possono riguardare condizioni congenite, quali la sindrome LQT360, LQT-CAV3, legata a mutazione della caveolina 3 61 e la sindrome LQT462
E' riportato che l'aumento di INaL è modulato dallo stato redox dell'ambiente intracellulare, che a sua volta viene modificato in condizioni di ipossia acuta: in tali condizioni l'aumento di INaL è associato a una diminuzione di INaT dei miociti ventricolari di cavia; questi effetti vengono annullati dalla somministrazione di composti antiossidanti, suggerendo che l'ipossia acuta agisca mediante formazione di ROS 63. Tale evidenza è supportata anche dall'aumento di INaL conseguente all'esposizione ad ipossia acuta in sistemi di espressione eterologa della subunità del canale NaV 1.5. 64 Inoltre, il trattamento di miociti ventricolari di ratto con H2O2 induce un significativo aumento della corrente persistente. 65;66 E' inoltre riportato che la formazione di perossinitriti, specie reattive derivanti dalla perossidazione dell'NO, è un passaggio cruciale per l'incremento di INaL indotto da lisofosfatidilcolina, un metabolita presente nel miocardio ischemico e noto agente pro-aritmico.67
L'incremento di INaL può avere importanti conseguenze sulla durata del potenziale d'azione, prolungando la fase 2 e facilitando l'insorgenza di EADs. Inoltre, anche se il flusso di sodio è di gran lunga inferiore a quello generato da INaT, il maggior tempo di attivazione della INaL permette di aumentare significativamente le moli di Na+ che entrano nella cellula ad ogni ciclo di attivazione. Il risultante aumento di Na+ intracellulare si riflette in uno spostamento del potenziale d'equilibrio dello scambiatore Na+/Ca2+ (ENCX) verso valori più negativi, aumentando la probabilità di funzionamento di NCX in reverse-mode: questo provoca un aumento del contenuto di calcio sistolico e diastolico nel miocita. L'aumento di calcio può aumentare la contrattilità, ma anche attivare vie di segnalazione intracellulari che possono indurre apoptosi o rimodellamento, aprendo la strada all'insufficienza cardiaca.
Oltre ai bloccanti selettivi della corrente di
sodio classici, come
L'inibizione della INaL riduce il sovraccarico di Na+ intracellulare e si traduce in una minore incidenza di EADs in miociti isolati da cuore con insufficienza contrattile 66;70. La riduzione del Ca2+ citosolico che ne consegue riduce la probabilità di apertura dei RyR e migliora la capacità del reticolo sarcoplasmatico di compartimentalizzare il Ca2+. L'inibizione del sovraccarico di Na+ derivante dal blocco di INaL ha inoltre un effetto positivo sul controllo del pH intracellulare, perché aiuta a mantenere il gradiente di Na+ necessario per l'espulsione dei protoni attraverso lo scambiatore Na+/H+. L'aumento del Na+ citosolico conduce anche a dissipazione del potenziale di membrana mitocondriale; la sua prevenzione aumenta quindi l'efficienza della fosforilazione ossidativa con effetti positivi sul metabolismo energetico.
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2025