|
|
| |
LA TERMODINAMICA
LA TERMODINAMICA E I SUOI PRINCIPI
Ogni sistema può essere osservato dal punto di vista dei trasferimenti di energia con l'ambiente esterno. E' questo il punto di vista della termodinamica, che studia le leggi con cui i corpi scambiano lavoro e calore con l'ambiente che li circonda.
La termodinamica:
si occupa delle trasformazioni di calore in lavoro che hanno luogo in tutti i motori termici
è fondata su 2 leggi, i cosiddetti principi della termodinamica, che hanno un carattere estremamente generale
PRIMO PRINCIPIO DELLA TERMODINAMICA
E' un'estensione del principio di conservazione dell'energia meccanica. Oltre al lavoro include anche il calore come forma di trasferimento dell'energia
SECONDO PRINCIPIO DELLA TERMODINAMICA
Stabilisce alcune limitazioni alla possibilità di trasformare calore in lavoro
LE MACCHINE TERMICHE
Come si fa a trasformare il calore in lavoro utile?
Con le macchine termiche che appunto sono macchine che utilizzano il calore per trasformarlo in lavoro. Dall'energia meccanica si passa sempre all'energia termica.
Le macchine termiche possono essere:
a combustione interna (la combustione avviene dentro)
a combustione esterna (la combustione avviene al di fuori del cilindro e del pistone)
a reazione a razzo
MACCHINE A COMBUSTIONE ESTERNA: LA MACCHINA DI NEWCOMEN


![]()
![]() 323h76d 2 323h76d bilanciere
323h76d 2 323h76d bilanciere
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() acqua di
acqua di
![]()
![]() refrigerazione
refrigerazione
![]()

![]() 323h76d 323h76d 323h76d stantuffo
323h76d 323h76d 323h76d stantuffo
![]()
![]()

![]() 323h76d 323h76d 1 vapore 1 323h76d secchio
che scende nel pozzo
323h76d 323h76d 1 vapore 1 323h76d secchio
che scende nel pozzo
![]()
![]()
![]()
![]()
![]()
![]()
![]() 323h76d 323h76d 323h76d 3 323h76d della
miniera
323h76d 323h76d 323h76d 3 323h76d della
miniera
![]()
![]()
![]()
![]()
![]() 323h76d 323h76d acqua
3
323h76d 323h76d acqua
3
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 323h76d 323h76d cilindro
323h76d 323h76d cilindro
323h76d vapore
![]()
![]()
![]()
![]()
![]()
![]()
![]() 323h76d bollitore
323h76d bollitore
![]()
![]()
![]()
![]()
![]()
![]()
![]() 323h76d 323h76d cioè
sorgente di calore
323h76d 323h76d cioè
sorgente di calore
323h76d fornace a temperatura elevata
![]()
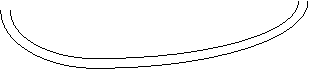
Il vapore prodotto dalla bollitura dell'acqua entra nel cilindro.
Lo stantuffo si alza per l'aumento di volume del gas.
Lo stantuffo fa abbassare il secchio, che entra nel pozzo
L'acqua di refrigerazione scende per mezzo di alcuni buchini che ci sono nel tubo
L'acqua fredda fa condensare il vapore contenuto nel cilindro
Il vapore diventa acqua.
A causa della diminuzione del volume lo stantuffo si abbassa.
Lo stantuffo fa alzare il secchio, che sale dal pozzo
L'acqua viene incanalata in un tubo
Il tubo riporta l'acqua nel bollitore
Nel punto 1, nel momento in cui il vapore ha fatto salire lo stantuffo, la temperatura è diminuita. Questo perché il vapore ha compiuto un lavoro ed ha ceduto un po' di energia.
Questa macchina aveva un rendimento molto basso, circa il 4%. Questo perché si hanno perdite di calore un po' ovunque: attraverso le pareti del bollitore, dei tubi etc. Ma soprattutto nel cilindro, perché prima che il cilindro possa essere riempito di vapore, deve essere riscaldato e quindi si hanno perdite di energia.
Una volta che il vapore diventa acqua la temperatura delle pareti del cilindro è diminuita. Di conseguenza nel 2° ciclo si avranno altre perdite di calore per riscaldare nuovamente il cilindro.
Il rendimento è il rapporto tra lavoro prodotto e calore fornito. In formula:
L
R = -------
Q
Il rendimento è sempre inferiore a 1, perché il calore che perdo è minore di quello fornito. Do 100 e guadagno più poco.
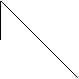
FUNZIONAMENTO DI TUTTE LE MACCHINE TERMICHE


![]()
![]()
![]()
![]()
![]() Sorgente di 323h76d 323h76d 323h76d 323h76d guadagno
Sorgente di 323h76d 323h76d 323h76d 323h76d guadagno
calore a
 temperatura Q fornito 323h76d MACCHINA
temperatura Q fornito 323h76d MACCHINA
elevata

![]()
![]()
![]()
323h76d 323h76d 323h76d Q perduto
![]()
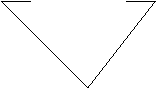
LA MACCHINA DI WATT
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 323h76d bilanciere
323h76d bilanciere
![]()
![]()
![]() 323h76d 323h76d 323h76d 323h76d 3
323h76d 323h76d 323h76d 323h76d 3
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 323h76d 323h76d 323h76d 323h76d 323h76d acqua
di
323h76d 323h76d 323h76d 323h76d 323h76d acqua
di
323h76d 323h76d 323h76d 323h76d 323h76d refrigerazione
secchio che scende
nel ![]()
![]()
![]()
![]()
![]()
pozzo della miniera
![]()
![]()
![]()
![]()
![]()
![]()
![]()

![]() 323h76d 323h76d 1 vapore vapore 2
323h76d 323h76d 1 vapore vapore 2
![]()
![]()
![]()
![]() 323h76d 323h76d 323h76d 2 323h76d 2° cilindro
323h76d 323h76d 323h76d 2 323h76d 2° cilindro
![]()
![]()
![]()
![]()
![]()
![]() 323h76d 323h76d 323h76d 323h76d acqua 3 4
323h76d 323h76d 323h76d 323h76d acqua 3 4
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 323h76d 323h76d 1° cilindro
323h76d 323h76d 1° cilindro
![]() 323h76d vapore
323h76d vapore
![]()
![]()
![]()
![]()
![]() 323h76d bollitore
323h76d bollitore
![]()
![]()
![]()
![]()
![]()
![]()
323h76d fornace
![]()

Il vapore prodotto dalla bollitura dell'acqua entra nel cilindro.
Lo stantuffo si alza per l'aumento di volume del gas.
Lo stantuffo fa abbassare il secchio, che entra nel pozzo
Il vapore entra in un 2° cilindro
L'acqua di refrigerazione scende per mezzo di alcuni buchini che ci sono nel tubo
L'acqua fredda fa condensare il vapore contenuto nel 2° cilindro
Il vapore diventa acqua.
A causa della diminuzione del volume nel 2° cilindro, diminuisce anche nel 1° cilindro e lo stantuffo si abbassa.
Lo stantuffo fa alzare il secchio, che sale dal pozzo
L'acqua del 2° cilindro viene incanalata in un tubo
Il tubo riporta l'acqua nel bollitore
Questa macchina rende di più di quella di Newcomen (5%), perché si è introdotto il 2° cilindro.
Facendo passare il vapore anche nel 2° cilindro, una volta che il vapore diventa acqua la temperatura delle pareti diminuisce solo nel 2° cilindro. Le pareti del 1° cilindro rimangono ad una temperatura costante. Di conseguenza nel 2° ciclo si avranno meno perdite di calore perché il vapore arriverà in un cilindro già caldo.
IL PRIMO PRINCIPIO DELLA TERMODINAMICA
Questo principio dice in modo preciso ciò che tutti sappiamo: l'energia non si crea né si distrugge, ma si trasforma.
Un sistema è un qualsiasi insieme di corpi che possiamo immaginare racchiusi in un contenitore di cellophane sottile, resistente e quasi inesistente.
Ogni sistema ha una ben definita energia interna che dipende dalle condizioni, cioè dallo stato in cui il sistema si trova.
L'energia interna si misura in joule, come tutte le forme di energia
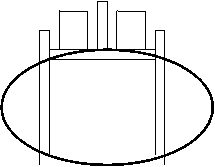
323h76d 323h76d 323h76d GAS 323h76d SISTEMA
![]()
![]()
323h76d 323h76d SORGENTE
![]()
Il sistema compie lavoro sull'ambiente esterno, perché alza il carico. Il lavoro è positivo.
Q = DU + L
DU = variazione dell'energia interna del sistema
L = lavoro compiuto dal sistema o sul sistema
Q= calore fornito dal sistema o sul sistema
APPLICAZIONE DEL PRIMO PRINCIPIO
![]()
![]()
![]() 323h76d Q sistema L 323h76d do calore
323h76d Q sistema L 323h76d do calore
![]()
![]() 323h76d 323h76d DU 323h76d 323h76d il sistema
varia la sua energia
323h76d 323h76d DU 323h76d 323h76d il sistema
varia la sua energia
323h76d 323h76d 323h76d 323h76d 323h76d interna
![]() 323h76d 323h76d 323h76d 323h76d 323h76d il
sistema fa un lavoro
323h76d 323h76d 323h76d 323h76d 323h76d il
sistema fa un lavoro
![]()
![]()
![]() Q = 100 J 323h76d 323h76d L = 80 J 323h76d Non si perde energia
perché
Q = 100 J 323h76d 323h76d L = 80 J 323h76d Non si perde energia
perché
![]()
![]() 323h76d DU = 20 J 323h76d 323h76d consideriamo
il sistema
323h76d DU = 20 J 323h76d 323h76d consideriamo
il sistema
323h76d 323h76d 323h76d 323h76d 323h76d isolato. Le perdite rimangono
![]() 323h76d 323h76d 323h76d 323h76d 323h76d come
energia interna
323h76d 323h76d 323h76d 323h76d 323h76d come
energia interna
Q > 0 DU > 0 L > 0
323h76d DU > 0 = Uf - Ui > 0, Uf > Ui
![]()
![]()
![]()
![]() Q = 100 J 323h76d 323h76d L = 100 J Il calore fornito è uguale
al
Q = 100 J 323h76d 323h76d L = 100 J Il calore fornito è uguale
al
323h76d 323h76d DU = 0 323h76d 323h76d lavoro svolto
![]()
![]()
![]()
323h76d 323h76d Ui = Uf
![]()
![]()
![]() Q = 100 J 323h76d 323h76d L = 120 J Per produrre più lavoro rubo
Q = 100 J 323h76d 323h76d L = 120 J Per produrre più lavoro rubo
![]()
![]() 323h76d DU = -20 J 323h76d 323h76d energia
interna al sistema. Le
323h76d DU = -20 J 323h76d 323h76d energia
interna al sistema. Le
323h76d 323h76d 323h76d 323h76d 323h76d molecole perdono energia
![]() 323h76d 323h76d 323h76d 323h76d 323h76d interna,
cioè velocità.
323h76d 323h76d 323h76d 323h76d 323h76d interna,
cioè velocità.
Q > 0 323h76d DU < 0 323h76d L > 0
![]()
![]()
![]() Q = 100 J 323h76d 323h76d L -50 J 323h76d Il lavoro si compie sul
siste-
Q = 100 J 323h76d 323h76d L -50 J 323h76d Il lavoro si compie sul
siste-
![]()
![]() 323h76d DU = 150 J 323h76d 323h76d ma,
cioè si comprime il pisto-
323h76d DU = 150 J 323h76d 323h76d ma,
cioè si comprime il pisto-
![]()
![]()
![]() 323h76d 323h76d 323h76d 323h76d 323h76d ne.
Le molecole aumentano
323h76d 323h76d 323h76d 323h76d 323h76d ne.
Le molecole aumentano
323h76d 323h76d 323h76d 323h76d 323h76d la loro energia interna
Q > 0 323h76d DU > 0 323h76d L < 0
![]()
![]()
![]() Q = -50 J 323h76d 323h76d L = 50 J 323h76d Il sistema cede calore a
spese
Q = -50 J 323h76d 323h76d L = 50 J 323h76d Il sistema cede calore a
spese
![]()
![]() 323h76d DU = -100 J 323h76d della sua energia interna; in
323h76d DU = -100 J 323h76d della sua energia interna; in
323h76d 323h76d 323h76d 323h76d 323h76d più svolge lavoro e perde ne
![]() 323h76d 323h76d 323h76d 323h76d 323h76d ancora
di più
323h76d 323h76d 323h76d 323h76d 323h76d ancora
di più
Q < 0 323h76d DU < 0 323h76d L > 0
![]()
![]()
![]() Q = -50 J 323h76d 323h76d L = -100 J Si toglie calore al sistema,
Q = -50 J 323h76d 323h76d L = -100 J Si toglie calore al sistema,
![]()
![]() 323h76d DU = 50 J 323h76d 323h76d ma
si compie anche un
323h76d DU = 50 J 323h76d 323h76d ma
si compie anche un
![]() 323h76d 323h76d 323h76d 323h76d 323h76d lavoro
sul sistema. Aumenta
323h76d 323h76d 323h76d 323h76d 323h76d lavoro
sul sistema. Aumenta
323h76d 323h76d 323h76d 323h76d 323h76d l'energia interna
Q < 0 323h76d DU > 0 L < 0
![]()
![]()
![]() Q = -100 J 323h76d 323h76d L = -50 J 323h76d Si toglie calore al
sistema,
Q = -100 J 323h76d 323h76d L = -50 J 323h76d Si toglie calore al
sistema,
![]() 323h76d DU = -50 J 323h76d 323h76d si
compie lavoro sul sistema,
323h76d DU = -50 J 323h76d 323h76d si
compie lavoro sul sistema,
![]() 323h76d 323h76d 323h76d 323h76d 323h76d ma
questo è poco. L'energia
323h76d 323h76d 323h76d 323h76d 323h76d ma
questo è poco. L'energia
![]() 323h76d 323h76d 323h76d 323h76d 323h76d interna
diminuisce
323h76d 323h76d 323h76d 323h76d 323h76d interna
diminuisce
Q < 0 323h76d DU < 0 323h76d L < 0
![]()
![]()
![]() Q = 100 J 323h76d 323h76d L = -100 J Si toglie calore, ma si
compie
Q = 100 J 323h76d 323h76d L = -100 J Si toglie calore, ma si
compie
323h76d 323h76d DU = 0 323h76d 323h76d un lavoro pari al calore tolto.
![]()
![]() 323h76d 323h76d 323h76d 323h76d 323h76d L'energia
interna non varia
323h76d 323h76d 323h76d 323h76d 323h76d L'energia
interna non varia
![]()
IL SECONDO PRINCIPIO DELLA TERMODINAMICA
E' sempre possibile trasformare completamente il lavoro in calore. Purtroppo non è sempre possibile il contrario; è possibile trasformare integralmente calore in lavoro. Il secondo principio della termodinamica afferma che non è possibile costruire una macchina termica che trasformi integralmente il calore in lavoro. Una parte del calore che il sistema assorbe deve essere "buttata via"
Per convertire calore in lavoro bisogna avere due sorgenti: una a temperatura maggiore e una a temperatura minore. Per calcolare il lavoro compiuto effettivamente dal sistema bisogna:
W = Q - Q
dove Q2 è la quantità di calore che una macchina termica assorbe alla temperatura elevata.
dove Q1 è la quantità di calore che una macchina termica "butta via" alla temperatura inferiore. Q1 deve essere sempre maggiore a 0, perché non esistono le macchine ideali. Quindi quanto è minore Q1, tanto più piccolo è lo spreco di calore.
Il rendimento è una grandezza che misura l'efficienza con cui una macchina termica converte il calore in lavoro.
W dal sistema
323h76d r = ----- ----- ----------
calore fornito
Sostituendo Q2-Q1 al posto di W si ottiene
323h76d Qfornito - Qperso Qfornito Qperso Qperso
R = ----- ----- ------------ = ----------- - ----------- = 1 - -----------
323h76d Qfornito Qfornito Qfornito Qfornito
Il rendimento di qualsiasi dispositivo che trasforma calore in lavoro è sempre minore di uno.
Il massimo rendimento di una macchina termica, che lavora tra due sorgenti di calore, è tanto più grande quanto è il dislivello di temperature.
MAPPA CONCETTUALE
![]()
![]()
![]() MACCHINE TERMICHE
MACCHINE TERMICHE
![]()
![]()
![]()
![]()
![]()
![]()
principi che ne regolano il comportamento
![]()
![]()
![]()
1° PRINCIPIO DELLA TERMODINAMICA 2° PRINCIPIO DELLA TERMODINAMI
![]()
![]()

Q = DU + L è un principio di 323h76d introduce il rendimento. Si tiene
![]() 323h76d conservazione
dell'energia conto delle
sue sorgenti a diversa
323h76d conservazione
dell'energia conto delle
sue sorgenti a diversa
![]() 323h76d 323h76d 323h76d 323h76d temperatura
323h76d 323h76d 323h76d 323h76d temperatura
![]()
![]()
323h76d 323h76d 323h76d RENDIMENTO
323h76d 323h76d 323h76d Carnot
![]()

macchine a:
combustione interna
combustione esterna
razzo
![]()
TRASFORMAZIONE ISOBARA (pressione costante)
323h76d 323h76d 323h76d 323h76d W = F s
![]()
![]()
![]()
![]()
![]()
![]() 323h76d F
323h76d F

![]()
![]() 323h76d Ds
323h76d Ds
![]()
323h76d A 323h76d B
A ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 323h76d 323h76d 323h76d 323h76d W = F s
323h76d 323h76d 323h76d 323h76d W = F s
![]()
![]() 323h76d 323h76d 323h76d 323h76d
323h76d 323h76d 323h76d 323h76d
![]()
![]() 323h76d 323h76d 323h76d 323h76d F
= peso del pistone + peso dei corpi
323h76d 323h76d 323h76d 323h76d F
= peso del pistone + peso dei corpi
![]() 323h76d 323h76d 323h76d 323h76d + peso dell'aria
323h76d 323h76d 323h76d 323h76d + peso dell'aria
323h76d 323h76d 323h76d 323h76d
![]()
B
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 323h76d 323h76d 323h76d 323h76d W
= F h F = P sup
323h76d 323h76d 323h76d 323h76d W
= F h F = P sup
![]()
![]()
![]()
![]()
![]()
![]() 323h76d h 323h76d 323h76d 323h76d W
= P sup h sup h = V
323h76d h 323h76d 323h76d 323h76d W
= P sup h sup h = V
![]()
![]()
![]()
![]() 323h76d 323h76d 323h76d V 323h76d V = differenza di volume
323h76d 323h76d 323h76d V 323h76d V = differenza di volume
![]()
![]()
![]() 323h76d 323h76d 323h76d 323h76d 323h76d W = P D V
323h76d 323h76d 323h76d 323h76d 323h76d W = P D V

INTERPRETAZIONE GRAFICA
![]()
P

323h76d 323h76d W
![]()
323h76d 323h76d DV 323h76d 323h76d V
323h76d 323h76d Vi Vf
TRASFORMAZIONE ISOCORA (volume costante)
323h76d 323h76d SORGENTE
![]()
P = Po (1 + 1/273t)
Non c'è lavoro perché la scatola è ermeticamente chiusa. W = 0
RAPPRESENTAZIONE GRAFICA
![]()
![]() 323h76d P
323h76d P
![]() 323h76d P2 323h76d 323h76d B
323h76d P2 323h76d 323h76d B
![]() 323h76d P1 323h76d 323h76d A
323h76d P1 323h76d 323h76d A
![]() 323h76d 323h76d 323h76d V1 323h76d V
323h76d 323h76d 323h76d V1 323h76d V
IL CICLO
![]() 323h76d P
323h76d P
323h76d 323h76d A 323h76d B
![]()
![]()
![]()
![]() P1
P1
scaldo e aggiungo W compiuto raffreddo e tolgo alcuni pesi
i pesi 323h76d dal ciclo

323h76d 323h76d D 323h76d C C - D = raffreddo
323h76d 323h76d W compiuto da C a D
![]()
323h76d 323h76d V1 323h76d V2 323h76d V
Q = DU + L
Wtotale = WAB - WCD
OSSERVAZIONI
Alla fine di un ciclo il gas termodinamico assume di nuovo le condizioni iniziali (stesso volume, stessa pressione, stesso gas); ha quindi di nuovo l'energia interna iniziale.
L'Uf è uguale al'Ui. Non varia l'energia interna perché stiamo lavorando in un ciclo, dove non c'è trasformazione. Infatti Q = DU + L vale per una trasformazione, non per un ciclo.
Per capire meglio come mai non avviene una trasformazione analizziamo cosa accade in un ciclo:
AB DU è positiva
BC 323h76d Q è uguale a DU. Quindi DU è negativa
CD DU è positiva
DA Q è uguale a DU. Quindi DU è negativa
DU rimane invariata, perché + - + - = 0
CONCLUSIONE
Q = DU + L
Q = 0 + L
Q = L
Q = calore totale scambiato nel ciclo
L = lavoro totale. Ovvero lavoro svolto sul sistema + lavoro svolto dal sistema
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2025