|
|
| |
Inquinanti principali
L'aria che respiriamo può essere contaminata da sostanze inquinanti provenienti da industrie, veicoli, centrali elettriche e molte altre fonti. Questi inquinanti rappresentano un grosso problema per gli effetti dannosi che possono avere nei confronti della salute o dell'ambiente in cui viviamo. Il loro impatto dipende da vari fattori, come ad esempio la quantità di inquinante dell'aria al quale si è esposti, la durata dell'esposizione e la pericolosità dell'inquinante stesso. Gli effetti sulla salute possono essere di piccola entità e reversibili (come un'irritazione agli occhi) oppure debilitanti (come un aggravamento dell'asma) o anche fatali (come il cancro).
In
questa parte del sito ho riportato varie informazioni inerenti i principali
inquinanti dell'aria: il monossido di carbonio, gli ossidi di zolfo, gli ossidi
di azoto, l'ozono, il particolato, il radon, il benzene, l'asbesto, gli
idrocarburi policiclici aromatici (IPA) ed il cloruro di vinile.
Per ognuno degli inquinanti sono descritte le caratteristiche principali, le
sorgenti, le modalità di diffusione, gli effetti sull'uomo e sull'ambiente (se
particolarmente rilevanti) ed infine le relative leggi e linee guida. 
Ossidi di zolfo SO
caratteristiche
Normalmente
gli ossidi di zolfo presenti in atmosfera sono l'anidride solforosa (SO ) e l'anidride solforica (SO ); questi composti vengono anche indicati con il termine
comune SOx.
L'anidride solforosa o biossido di zolfo è un gas incolore, irritante, non
infiammabile, molto solubile in acqua e dall'odore pungente. Dato che è più
pesante dell'aria tende a stratificarsi nelle zone più basse.
Rappresenta l'inquinante atmosferico per eccellenza essendo il più diffuso, uno
dei più aggressivi e pericolosi e di gran lunga quello più studiato ed emesso
in maggior quantità dalle sorgenti antropogeniche.
Deriva dalla ossidazione dello zolfo nel corso dei processi di combustione delle sostanze che contengono questo elemento sia come impurezza (come i combustibili fossili) che come costituente fondamentale.
Dall'ossidazione dell'anidride solforosa si origina l'anidride solforica o triossido di zolfo che reagendo con l'acqua, sia liquida che allo stato di vapore, origina rapidamente l'acido solforico, responsabile in gran parte del fenomeno delle piogge acide. Dato che la reazione di ossidazione che conduce alla formazione dell'anidride solforica è molto lenta, e data la reattività di questo composto con l'acqua, in genere la concentrazione del triossido di zolfo varia fra l'1 e il 5% della concentrazione del biossido di zolfo (che viene considerato l'inquinante di riferimento).
Fonti inquinanti
Le
emissioni naturali di biossido di zolfo sono principalmente dovute all'attività
vulcanica (circa 20 milioni di tonnellate l'anno).
Le emissioni antropogeniche rappresentano più di 150 milioni di tonnellate
all'anno e sono dovute principalmente ai processi di combustione dei
combustibili fossili e liquidi (carbone, petrolio, gasolio); oltre il 90% del
biossido di zolfo viene prodotto nell'emisfero Nord.
Il carbon fossile ha un contenuto di zolfo che varia dallo 0,1 al 6% e il
petrolio gre 616f52g ggio dallo 0,05 al 4,5%. Oltre il 90% dello zolfo presente nel
combustibile viene trasformato in biossido di zolfo (lo 0,5-2% viene
trasformato in anidride solforica ed il resto rimane nelle ceneri sotto forma
di solfati).
Rilevanti
sono anche le emissioni nei processi di produzione dell'acido solforico, nella
lavorazione di molte materie plastiche, nella desolforazione dei gas naturali,
nell'arrostimento delle piriti, nell'incenerimento dei rifiuti; l'apporto
inquinante dato dalle emissioni dei mezzi di trasporto appare invece
trascurabile.
L'emissione di biossido di zolfo in Italia è approssimativamente dovuta per il
5% al riscaldamento domestico, per il 40% ai processi industriali comprese le
combustioni e per il 50% alla produzione di energia elettrica ad opera delle
centrali termoelettriche; assieme le altre sorgenti contribuiscono per un
valore pari al 5%.
Da notare che i combustibili a basso tenore di zolfo non sono facilmente
disponibili e i processi di desolforazione sono costosi. Solo una maggiore
sensibilizzazione dell'opinione pubblica sul problema delle piogge acide negli
ultimi anni, sembra stia spingendo verso interventi nel settore.
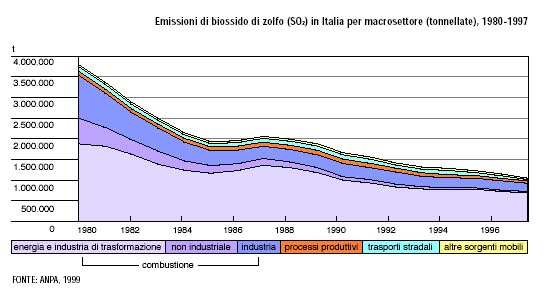
Pur essendo notevolmente diminuite dagli anni ottanta, le emissioni di biossido di zolfo permangono estremamente elevate: più di un milione di tonnellate all'anno.
diffusione
La
concentrazione di fondo è stata valutata attorno a 0,2-0,5 µg/mc, mentre nelle
aree urbane si possono raggiungere i 50 µg/mc; nelle grandi città
industrializzate ed in via di sviluppo vengono spesso rilevati anche livelli di
300 µg/mc (dati dell'Organizzazione Mondiale della Sanità, 1998).
Il biossido di zolfo permane in atmosfera per 1-4 giorni subendo reazioni di
trasformazione e principalmente l'ossidazione ad acido solforico che ricade in
forma di nebbie o piogge acide. Gli ossidi di zolfo di notte vengono anche
assorbiti dalle goccioline di acqua presenti nell'aria dando origine ad un
aerosol che determina una foschia mattutina.
A
causa della grande reattività del biossido di zolfo, le concentrazioni negli
ambienti interni sono generalmente molto basse (almeno la metà di quelle
esterne). Inoltre nei mesi invernali, quando il livello di concentrazione
all'esterno tende ad aumentare per effetto del maggior utilizzo del
riscaldamento domestico, le abitazioni restano chiuse per il freddo e pertanto
la concentrazione indoor risulta più contenuta.
Nelle abitazioni sono inoltre presenti numerose sostanze ed oggetti che
assorbono il biossido di zolfo (oggetti in pelle, coperte di lana) e
contribuiscono a diminuire la concentrazione dell'inquinante. Una precauzione
da osservare durante gli episodi acuti di smog è infatti quella di rimanere
chiusi nelle abitazioni.
Nel corso degli ultimi anni, a causa degli interventi che sono stati adottati
per il miglioramento della qualità dei combustibili e per la diffusione della
metanizzazione degli impianti di riscaldamento, l'emissione degli ossidi di
zolfo nelle aree urbane dei Paesi Occidentali si è notevolmente ridotta, per
cui l'importanza del biossido di zofo come inquinante è leggermente diminuita
(almeno nei centri abitati).
Effetti sull' uomo
Per
l'elevata solubilità in acqua il biossido di zolfo viene facilmente assorbito
dalle mucose del naso e del tratto superiore dell'apparato respiratorio (questo
rappresenta una fortuna dato che solo quantità molto ridotte possono
raggiungere gli alveoli polmonari). L'alta reattività lo rende un composto
estremamente irritante. E' stato comunque notato un effetto sinergico con le
polveri sospese per la capacità che queste hanno di veicolare gli inquinanti
nelle zone più profonde dell'apparato respiratorio.
A basse concentrazioni gli effetti del biossido di zolfo sono principalmente
legati a patologie dell'apparato respiratorio come bronchiti, asma e tracheiti
e ad irritazioni della pelle, degli occhi e delle mucose.
Analisi
epidemiologiche hanno evidenziato un aumento dei ricoveri ospedalieri, specie
di anziani e bambini, a concentrazioni superiori a 0,3 mg/mc. Già a
concentrazioni di 0,06 mg/mc come valore medio annuale si verificano episodi di
bronchite e infezioni alle prime vie respiratorie.
Il caratteristico odore pungente del biossido di zolfo viene percepito dal naso
alla concentrazione di 0,8-2,6 mg/mc. A questi livelli bisogna infilare la
maschera antigas o, trattenendo il respiro, raggiungere una zona non
contaminata. Per brevi periodi, in assenza di maschera, ci si può proteggere
anche tenendo sul naso e sulla bocca un panno umido.
Brevi esposizioni di 10' a concentrazioni di 3 mg/mc provocano un aumento del
ritmo respiratorio e del battito cardiaco; concentrazioni di 25 mg/mc provocano
irritazioni agli occhi, al naso ed alla gola, oltre ad un aumento della frequenza
cardiaca. Concentrazioni maggiori di 5 g/mc producono asfissia tossica con
morte per collasso cardiocircolatorio.
Effetti sull' ambiente
L'azione
principale operata ai danni dell'ambiente da parte degli ossidi di zolfo
consiste nell'acidificazione delle precipitazioni meteorologiche con la
conseguente compromissione dell'equilibrio degli ecosistemi interessati. Gli
effetti corrosivi dell'acido solforico si riscontrano anche sui materiali da
costruzione, sui metalli e sulle vernici.
L'acido solforico trasforma i carbonati insolubili dei monumenti e delle opere
d'arte in solfati solubili che vengono dilavati per azione della pioggia. (Per
maggiori informazioni consiglio di fare riferimento alla parte del sito che
tratta delle piogge acide).
Il biossido di
zolfo a basse concentrazioni provoca un rallentamento nella crescita delle
piante, mentre ad alte concentrazione ne provoca la morte alterandone la
fisiologia in modo irreparabile.
Nelle foglie il biossido di zolfo viene trasformato in acido solforoso e
solfiti, da questi per ossidazione si generano i solfati (la forma in cui lo
zolfo viene metabolizzato nelle piante). Quando il livello di anidride
solforosa nell'aria diviene insostenibile, nelle foglie si accumulano
inutilizzati i solfiti che ad alta concentrazione causano la distruzione della
clorofilla, il collasso delle cellule e la necrosi dei tessuti. Le foglie
presentano fra i margini e le nervature delle aree irregolari di colore bianco,
giallo o marrone, che presentano necrosi; negli aghi delle conifere diviene
marrone l'apice delle foglie. Questi effetti aumentano quando si è in presenza
di un'umidità relativa elevata, vi sono alte temperature, c'è un'intensa
luminosità ed anche nel caso in cui le piante siano vecchie.
L'effetto di una esposizione prolungata a concentrazioni di anidride solforosa
incapaci di causare sintomi evidenti è più difficile da rilevare: consiste in
una serie di alterazioni fisiologiche fra le quali la riduzione della crescita
e della riproduzione e la senescenza anticipata.
L'effetto sulle piante è particolarmente accentuato quando l'anidride solforosa
si trova in presenza di ozono (sinergismo).
Il biossido di
zolfo a basse concentrazioni provoca un rallentamento nella crescita delle
piante, mentre ad alte concentrazione ne provoca la morte alterandone la
fisiologia in modo irreparabile.
Nelle foglie il biossido di zolfo viene trasformato in acido solforoso e
solfiti, da questi per ossidazione si generano i solfati (la forma in cui lo
zolfo viene metabolizzato nelle piante). Quando il livello di anidride
solforosa nell'aria diviene insostenibile, nelle foglie si accumulano
inutilizzati i solfiti che ad alta concentrazione causano la distruzione della
clorofilla, il collasso delle cellule e la necrosi dei tessuti. Le foglie presentano
fra i margini e le nervature delle aree irregolari di colore bianco, giallo o
marrone, che presentano necrosi; negli aghi delle conifere diviene marrone
l'apice delle foglie. Questi effetti aumentano quando si è in presenza di
un'umidità relativa elevata, vi sono alte temperature, c'è un'intensa
luminosità ed anche nel caso in cui le piante siano vecchie.
L'effetto di una esposizione prolungata a concentrazioni di anidride solforosa
incapaci di causare sintomi evidenti è più difficile da rilevare: consiste in
una serie di alterazioni fisiologiche fra le quali la riduzione della crescita
e della riproduzione e la senescenza anticipata.
L'effetto sulle piante è particolarmente accentuato quando l'anidride solforosa
si trova in presenza di ozono (sinergismo).

Come si può chiaramente vedere dalla foto, un'esposizione anche breve al biossido di zolfo provoca notevoli danni a livello fogliare.
Ossidi di azoto NO
Caratteristiche
Pur essendo presenti in atmosfera diverse specie di ossidi di ozoto, per quanto riguarda l'inquinamento dell'aria si fa quasi esclusivamente riferimento al termine NOx che sta ad indicare la somma pesata del monossido di azoto (NO) e del biossido di azoto (NO
L'ossido di azoto (NO) è un gas incolore, insapore ed inodore; è anche chiamato ossido nitrico. E' prodotto soprattutto nel corso dei processi di combustione ad alta temperatura assieme al biossido di azoto (che costituisce meno del 5% degli NOx totali emessi). Viene poi ossidato in atmosfera dall'ossigeno e più rapidamente dall'ozono producendo biossido di azoto. La tossicità del monossido di azoto è limitata, al contrario di quella del biossido di azoto che risulta invece notevole. Il biossido di azoto è un gas tossico di colore giallo-rosso, dall'odore forte e pungente e con grande potere irritante; è un energico ossidante, molto reattivo e quindi altamente corrosivo. Esiste nelle due forme N O (forma dimera) e NO che si forma per dissociazione delle molecole dimere. Il colore rossastro dei fumi è dato dalla presenza della forma NO (che è quella prevalente). Il ben noto colore giallognolo delle foschie che ricoprono le città ad elevato traffico è dovuto per l'appunto al biossido di azoto. Rappresenta un inquinante secondario dato che deriva, per lo più, dall'ossidazione in atmosfera del monossido di azoto. Il biossido di azoto svolge un ruolo fondamentale nella formazione dello smog fotochimico in quanto costituisce l'intermedio di base per la produzione di tutta una serie di inquinanti secondari molto pericolosi come l'ozono, l'acido nitrico, l'acido nitroso, gli alchilnitrati, i perossiacetililnitrati, ecc. (per maggiori informazioni consiglio di fare riferimento alla parte del sito che tratta dello smog fotochimico).
Si stima che gli ossidi di azoto contribuiscano per il 30% alla formazione delle piogge acide (il restante è imputabile al biossido di zolfo e ad altri inquinanti). Da notare che gli NOx vengono per lo più emessi da sorgenti al suolo e sono solo parzialmente solubili in acqua, questo influenza notevolmente il trasporto e gli effetti a distanza.
Fonti inquinanti
Su scala globale
si stima che le emissioni di ossidi di azoto naturali ed antropogeniche siano
dello stesso ordine di grandezza (circa 200 milioni di tonnellate).
Le sorgenti naturali sono costituite essenzialmente dalle decomposizioni
organiche anaerobiche che riducono i nitrati a nitriti; i nitriti in ambiente
acido formano acido nitroso che, essendo instabile, libera ossidi di azoto. Da
segnalare anche l'azione dei fulmini, gli incendi e le emissioni vulcaniche.
La principale fonte antropogenica di ossido di azoto è data dalle combustioni ad alta temperatura, come quelle che avvengono nei motori degli autoveicoli: l'elevata temperatura che si origina durante lo scoppio provoca la reazione fra l'azoto dell'aria e l'ossigeno formando monossido di azoto.
La quantità
prodotta è tanto più elevata quanto maggiore è la temperatura di combustione e
quanto più veloce è il successivo raffreddamento dei gas prodotti, che
impedisce la decomposizione in azoto ed ossigeno.
Da notare che le miscele "ricche" (cioè con poca aria) danno luogo ad emissioni
con basso tenore di monossido di azoto (ma elevate emissioni di idrocarburi e
monossido di carbonio per effetto di combustioni incomplete) a causa della
bassa temperatura raggiunta nella camera di combustione. Miscele "povere" (cioè
con elevata quantità di aria) danno ancora luogo a basse concentrazioni di NO
nelle emissioni, ma impediscono una buona resa del motore perché l'eccesso di
aria raffredda la camera di combustione. Quando i fumi vengono mescolati con
aria allo scarico si forma una significativa quantità di biossido di azoto per
ossidazione del monossido ad opera dell'ossigeno.
In generale i motori diesel emettono più ossidi di azoto e particolati (fumo)
rispetto ai motori a benzina, i quali però emettono più ossido di carbonio e
idrocarburi.
Si stima che in Italia vengano emesse in atmosfera circa 2 milioni di tonnellate
all'anno di ossidi di azoto, di cui circa la metà è dovuta al traffico degli
autoveicoli.
Altre importanti fonti di ossidi di azoto sono gli impianti termici e le
centrali termoelettriche; le quantità emesse sono comunque relativamente minori
dato che nel corso della combustione vengono raggiunte temperature di fiamma
più basse. Sorgenti antropogeniche di ossidi di azoto sono inoltre la
produzione dei fertilizzanti azotati, la produzione di acido nitrico per
ossidazione dell'ammoniaca e la fabbricazione degli esplosivi, tutti i processi
chimici che impiegano acido nitrico (come ad esempio la dissoluzione di
metalli).
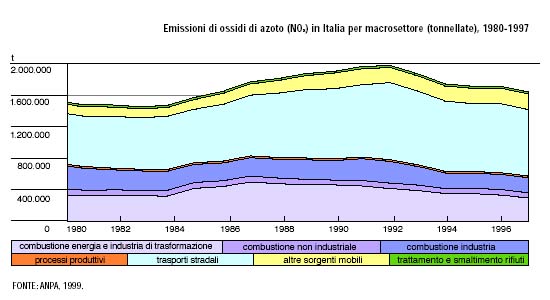
diffusione
Negli ultimi anni
le emissioni antropogeniche di ossidi di azoto sono aumentate enormemente,
soprattutto a causa dell'aumento del traffico veicolare, e questo ha comportato
di conseguenza un aumento dei livelli di concentrazione nelle aree urbane.
La concentrazione di fondo del monossido di azoto in atmosfera varia da 0,2 a
10 µg/mc; nell'aria inquinata la concentrazione di NO è in genere di 50-750 ppb
(62-930 µg/mc).
Nel caso in cui l'inquinamento sia dovuto ad una casualità fortuita, la
concentrazione dell'inquinante nell'aria cala rapidamente nel giro di 2-5
giorni: infatti l'ossido di azoto viene sempre rimosso per ossidazione.
Nelle atmosfere
inquinate in modo continuativo (in genere dagli autoveicoli) si assiste ad un
ciclo giornaliero di formazione di inquinanti secondari: il monossido di azoto
viene ossidato tramite reazioni fotochimiche (catalizzate dalla luce) a
biossido di azoto; si forma così una miscela NO-NO , che raggiunge il picco di
concentrazione nelle zone e nelle ore di traffico più intenso. Attraverso una
serie di reazioni, ancora catalizzate dalla luce solare, si giunge alla
formazione di ozono e di composti organici ossidanti (vedi smog fotochimico).
Durante la notte queste sostanze decadono formando composti organici nitrati,
perossidi ed aerosol acidi. Una situazione del genere si verifica specialmente
nelle città ad elevato traffico e molto soleggiate come ad esempio Los Angeles,
Città del Messico, Santiago del Cile (nella foto a lato), Roma, ecc. Le città
sembrano avvolte che una nube di inquinanti che, oltre a provocare una
diminuzione della visibilità costituiscono un pericolo per la salute dei
soggetti più deboli come i bambini, gli anziani e gli asmatici. La situazione
può diventare estremamente seria se fenomeni di intrappolamento ed assenza di
vento impediscono alla nube di disperdersi.
La concentrazione ambientale del biossido di azoto oscilla tra 1 e 9 µg/mc; nei
Paesi Occidentali la media annuale è compresa fra 20 e 90 µg/mc, mentre nelle
città in genere non supera i 40 µg/mc.
Negli ambienti indoor la concentrazione di ossidi di azoto risulta più elevata nelle cucine per le combustioni aperte dei fornelli (spesso può arrivare a concentrazioni più elevate di quelle esterne). La diminuzione di questi inquinanti risulta comunque estremamente rapida non appena vien meno la causa della loro produzione.
effetti sull' uomo
L'azione
sull'uomo dell'ossido di azoto è relativamente blanda; inoltre, a causa della
rapida ossidazione a biossido di azoto, si fa spesso riferimento esclusivo solo
a quest'ultimo inquinante, in quanto risulta molto più tossico del monossido.
Il biossido di azoto è un gas irritante per le mucose e può contribuire
all'insorgere di varie alterazioni delle funzioni polmonari, bronchiti
croniche, asma ed enfisema polmonare. Lunghe esposizioni anche a basse
concentrazioni provocano una drastica diminuzione delle difese polmonari con
conseguente aumento di rischio di affezioni alle vie respiratorie.
L'azione
sull'uomo dell'ossido di azoto è relativamente blanda; inoltre, a causa della
rapida ossidazione a biossido di azoto, si fa spesso riferimento esclusivo solo
a quest'ultimo inquinante, in quanto risulta molto più tossico del monossido.
Il biossido di azoto è un gas irritante per le mucose e può contribuire
all'insorgere di varie alterazioni delle funzioni polmonari, bronchiti
croniche, asma ed enfisema polmonare. Lunghe esposizioni anche a basse
concentrazioni provocano una drastica diminuzione delle difese polmonari con
conseguente aumento di rischio di affezioni alle vie respiratorie.
effetti sull' ambiente
L'inquinamento da
biossido di azoto ha un impatto sulla vegetazione di minore entità rispetto al
biossido di zolfo. In alcuni casi, brevi periodi di esposizione a basse
concentrazioni possono incrementare i livelli di clorofilla; lunghi periodi
causano invece la senescenza e la caduta delle foglie più giovani.
Il meccanismo principale di aggressione comunque è costituito
dall'acidificazione del suolo (vedi fenomeno delle piogge acide); gli
inquinanti acidi causano un impoverimento del terreno per la pedita di ioni
calcio, magnesio, sodio e potassio e conducono alla liberazione di iono
metallici tossici per le piante.
Da notare che l'abbassamento del pH compromette anche molti processi microbici
del terreno, fra cui l'azotofissazione.
Gli ossidi di azoto e i loro derivati danneggiano anche edifici e monumenti, provocando un invecchiamento accelerato in molti casi irreversibile.
Monossido di carbonio CO
Caratteristiche
L'ossido
di carbonio CO) o monossido
di carbonio è
un gas incolore, inodore, infiammabile, e molto tossico. Si forma durante le
combustioni delle sostanze organiche, quando sono incomplete per difetto di
aria (cioè per mancanza di ossigeno). Le emissioni naturali e quelle
antropogeniche sono oramai dello stesso ordine di grandezza, e questo fa
chiaramente comprendere quale sia il trend inquinante che si è instaurato nel
corso dell'ultimo secolo. Il monossido di carbonio è estremamente diffuso
soprattutto nelle aree urbane a causa dell'inquinamento prodotto dagli scarichi
degli autoveicoli.
Gli effetti sull'ambiente sono da considerarsi trascurabili, mentre gli effetti
sull'uomo sono particolarmente pericolosi. La sua pericolosità è dovuta alla
formazione con l'emoglobina del sangue di un composto fisiologicamente
inattivo, la carbossiemoglobina, che impedisce l'ossigenazione dei
tessuti. A basse concentrazioni provoca emicranie, debolezza diffusa, giramenti
di testa; a concentrazioni maggiori può provocare esiti letali.
fonti inquinanti
Le principali emissioni naturali sono dovute agli incendi delle foreste, alle eruzioni dei vulcani, alle emissioni da oceani e paludi e all'ossidazione del metano e degli idrocarburi in genere emessi naturalmente in atmosfera.
La fonte principale di emissione da parte dell'uomo è costituita dall'utilizzo dei combustibili fossili per i motori a scoppio degli autoveicoli e per le attività industriali (soprattutto impianti siderurgici e raffinerie di petrolio).
Escudendo
l'anidride carbonica, la quantità di ossido carbonio che viene emesso dai
processi di combustione che avvengono negli autoveicoli è circa 10 volte
maggiore di quella degli altri inquinanti. A seconda del regime di marcia la
concentrazione usuale che si riscontra nei gas di scarico delle automobili
varia fra il 3,5 e il 10%. Le concentrazioni più elevate nei gas di scarico si
riscontrano quando il motore funziona al minimo, a regimi più elevati la
produzione di CO è nettamente minore. Per questo motivo nelle zone urbane dove
il traffico procede a rilento e dove le fermate ai semafori sono frequenti, la
concentrazione del CO può raggiungere punte particolarmente elevate. I motori
Diesel, funzionando con maggiori quantità di aria, garantiscono una combustione
più completa ed emettono minori quantità di CO rispetto ai motori a benzina (in
compenso emettono più particolati). Negli ultimi anni la quantità di CO emessa
dagli scarichi degli autoveicoli è diminuita per il miglioramento
dell'efficienza dei motori, per il controllo obbligatorio delle emissioni e per
il crescente utilizzo delle marmitte catalitiche.
Per quanto riguarda le attività industriali c'è da sottolineare il fatto che il
CO è un discreto combustibile e la sua emissione con i gas di combustione costituisce
una perdita energetica, per questo si cerca sempre di attuare le combustioni in
eccesso di aria, migliorandole come resa e di conseguenza limitando l'emissione
di ossido di carbonio. Combustioni incomplete possono avvenire solo quando gli
impianti non vengono manutenzionati, oppure all'avviamento degli impianti,
quando la combustione avviene in difetto di aria per brevi periodi. Fra i
processi industriali che provocano emissioni rilevanti di CO in atmosfera, le
principali sono le emissioni degli impianti siderurgici, dove si impiega il
coke per la riduzione del materiale ferroso, o nelle conversioni, dove si
impiega l'ossigeno per ossidare il carbonio contenuto nelle ghise per
convertirle in acciaio o per abbassare il tasso di carbonio. Altre fonti sono
le industrie petrolchimiche che producono il gas di sintesi (una miscela di CO
e idrogeno) che serve per le produzioni di importanti composti chimici
sintetici, e le raffinerie di petrolio
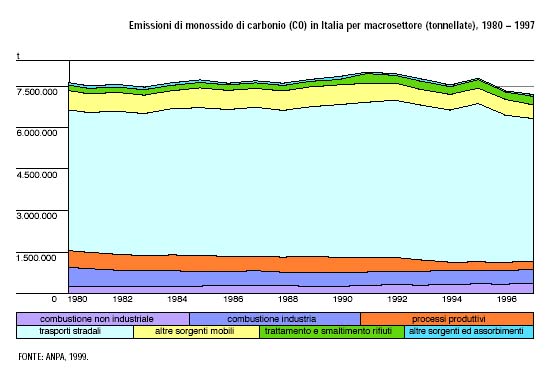
diffusione
In
atmosfera la concentrazione di fondo del monossido di carbonio è di 0,1-0,2 ppm
nell'emisfero nord e di 0,04-0,06 ppm nell'emisfero sud, a dimostrazione
dell'importanza del consumo di combustibili come fonte dell'inquinamento.
Nell'aria inquinata di aree intensamente urbanizzate può raggiungere 1-10 ppm,
in alcune gallerie stradali sono state rilevate concentrazioni di 500 ppm. Il
CO permane in atmosfera per circa 3-4 mesi e viene rimosso attraverso reazioni
di ossidazione ad anidride carbonica o attraverso reazioni fotochimiche
coinvolgenti il metano e i radicali OH. Per questa sua scarsa reattività viene
spesso utilizzato come tracciante dell'andamento temporale degli inquinanti a
livello del suolo.
Negli ambienti interni il monossido di carbonio proviene dalle stufe a gas, a
legna, ad olio combustibile, dai fornelli, dalle sigarette e dalle automobili
accese in garage. In alcuni casi sono stati rilevate anche concentrazioni di 50
ppm per operazioni di movimentazione dell'auto in garage, che confina di norma
con l'abitazione, quando all'esterno la concentrazione misurata era al massimo
di 1 ppm.
effetti sull' uomo
Per le sue caratteristiche l'ossido di carbonio rappresenta un inquinante molto insidioso, soprattutto nei luoghi chiusi dove si può accumulare in concentrazioni letali. Tali situazioni sono purtroppo frequenti e innumerevoli sono i casi di avvelenamento e gli incidenti anche mortali imputabili alle stufe o agli scaldabagni difettosi o non controllati. Essendo il CO incolore, insapore, inodore e non irritatante, può causare morti accidentali senza che le vittime si rendano conto di quel che sta loro succedendo. Frequenti sono pure i suicidi provocati dai gas di scarico delle automobili nei locali non aerati.
Una
volta respirato, il CO si lega all'emoglobina con una affinità che è 220 volte
superiore a quella dell'ossigeno e formando un composto inattivo
fisiologicamente che viene chiamato carbossiemoglobina. Questa sostanza, al
contrario dell'emoglobina, non è in grado di garantire l'ossigenazione ai
tessuti, in particolare al cervello ed al cuore. La morte sopravviene pertanto
per asfissia. L'effetto del CO risulta maggiore in altitudine, per la ridotta
percentuale di ossigeno nell'aria. In caso di intossicazione bisogna
immediatamente portare all'aria aperta il soggetto colpito, perché la
respirazione di aria arricchita di ossigeno aiuta l'eliminazione del CO dalla
carbossiemoglobina.
Una concentrazione di CO nell'aria pari a 2000-4000 ppm (0,2%-0,4%) provoca la
morte in circa 15 minuti, dopo aver provocato perdita di conoscenza. In
presenza di 1000 ppm si sopravvive circa 90 minuti. I primi sintomi
dell'avvelenamento sono l'emicrania e un senso di vertigine, purtroppo il gas
provoca anche sonnolenza e questo impedisce spesso alle vittime di avvertire il
pericolo e di aerare il locale.
A causa del traffico automobilistico la popolazione urbana è spesso soggetta a
lunghe esposizioni a basse concentrazioni. La lenta intossicazione da ossido di
carbonio prende il nome di ossicarbonismo e si manifesta con sintomi nervosi e
respiratori. Nel sangue è presente una percentuale di carbossiemoglobina che
dipende dalla concentrazione di CO alla quale una persona è esposta: per ogni
ppm di CO presente in aria, lo 0,16% di emoglobina viene trasformato in
carbossiemoglobina; sono necessarie però alcune ore perchè si raggiunga la
massima saturazione. In proporzione periodi di esposizione più brevi formano
meno carbossiemoglobina. Sono considerate fisiologiche concentrazioni di carbossiemoglobina
minori dell'1% dell'emoglobina circolante nel sangue. Quando nell'aria la
concentrazione di CO è di 12-31 ppm si arriva al 2-5% di carbossiemoglobina e
si manifestano i primi segni con aumento delle pulsazioni cardiache, aumento
della frequenza respiratoria e disturbi psicomotori (nei guidatori di auto si
allungano in modo pericoloso i tempi di reazione). A 100 ppm di esposizione per
diverse ore (come nel caso di lunghe soste in gallerie stradali) compaiono
vertigini, cefalea e senso generale di spossatezza, che possono essere seguiti
da collasso.
Nei fumatori la percentuale di carbossiemoglobina presente nel sangue può
variare dal 6% in fumatori moderati, sino al 10% in accaniti fumatori di
sigarette che siano esposti anche ad una concentrazione esterna di CO di circa
40 ppm per 1 ora, quando al confronto un non fumatore ha un aumento di
carbossiemoglobina da 1,6 al 2,6%.
L'esposizione a monossido di carbonio comporta inoltre l'aggravamento delle
malattie cardiovascolari, un peggioramento dello stato di salute nelle persone
sane ed un aggravamento delle condizioni circolatorie in generale.
Particolato atmosferico
Caratteristiche
Spesso
il particolato rappresenta l'inquinante a maggiore impatto ambientale nelle
aree urbane, tanto da indurre le autorità competenti a disporre dei blocchi del
traffico per ridurne il fenomeno.
Le particelle sospese sono sostanze allo stato solido o liquido che, a causa
delle loro piccole dimensioni, restano sospese in atmosfera per tempi più o
meno lunghi; le polveri totali sospese o PTS vengono anche indicate come PM (Particulate Matter).
Il particolato nell'aria può essere costituito da diverse sostanze: sabbia,
ceneri, polveri, fuliggine, sostanze silicee di varia natura, sostanze
vegetali, composti metallici, fibre tessili naturali e artificiali, sali,
elementi come il carbonio o il piombo, ecc.
In base alla natura e alle dimensioni
delle particelle possiamo distinguere:
- gli aerosol, costituiti da particelle solide o liquide sospese in aria
e con un diametro inferiore a 1 micron (1 µm);
- le foschie, date da goccioline con diametro inferiore a 2 micron;
- le esalazioni, costituite da particelle solide con diametro inferiore ad
1 micron e rilasciate solitamente da processi chimici e metallurgici;
- il fumo, dato da particelle solide di solito con diametro
inferiore ai 2 µm e trasportate da miscele di gas;
- le polveri (vere e proprie), costituite da particelle solide con
diametro fra 0,25 e 500 micron;
- le sabbie, date da particelle solide con diametro superiore ai 500
µm.
Le particelle
primarie
sono quelle che vengono emesse come tali dalle sorgenti naturali ed antropiche,
mentre le secondarie si originano da una serie di
reazioni chimiche e fisiche in atmosfera. Le particelle
fini sono
quelle che hanno un diametro inferiore a 2,5 µm, le altre sono dette grossolane. Da notare che il
particolato grossolano è costituito esclusivamente da particelle primarie.
Le polveri PM rappresentano il
particolato che ha un diametro inferiore a 10 micron e vengono anche dette polveri
inalabili
perché sono in grado di penetrare nel tratto superiore dell'apparato
respiratorio (dal naso alla laringe).
Le polveri toraciche sono quelle in grado di
raggiungere i polmoni.
Le polveri PM costituiscono circa il
60% delle PM e rappresentano il
particolato che ha un diametro inferiore a 2,5 micron. Le PM sono anche dette polveri respirabili perché possono penetrare
nel tratto inferiore dell'apparato respiratorio (dalla trachea fino agli
alveoli polmonari).
Fonti inquinanti
Le polveri si originano sia da fonti naturali che antropogeniche. Le polveri fini derivano principalmente da processi di combustione (particolato primario cioè prodotto direttamente) e da prodotti di reazione dei gas (particolato secondario); la frazione grossolana delle polveri si origina in genere da processi meccanici (solo p. primario).
Le principali fonti naturali di particolato primario sono le eruzioni vulcaniche, gli incendi boschivi, l'erosione e la disgregazione delle rocce, le piante (pollini e residui vegetali), le spore, lo spray marino e i resti degli insetti.
Il particolato naturale secondario è costituito da particelle fini che si originano in seguito alla ossidazione di varie sostanze quali: il biossido di zolfo e l'acido solfidrico emessi dagli incendi e dai vulcani; gli ossidi di azoto liberati dai terreni; i terpeni (idrocarburi) emessi dalla vegetazione.
Il particolato primario di origine
antropica è
invece dovuto: all'utilizzo dei combustibili fossili (riscaldamento domestico,
centrali termoelettriche, ecc.); alle emissioni degli autoveicoli; all'usura
dei pneumatici, dei freni e del manto stradale; a vari processi industriali
(fonderie, miniere, cementifici, ecc.). Da segnalare anche le grandi quantità
di polveri che si possono originare in seguito a varie attività agricole.
Le polveri secondarie antropogeniche sono invece dovute essenzialmente
all'ossidazione degli idrocarburi e degli ossidi di zolfo e di azoto emessi
dalle varie attività umane.

Un'impressionante eruzione dell'Etna ripresa dal satellite. Come si può vedere l'emissione di gas e polveri è enorme.
[NCI1] Diffusione
Si
stima che ogni giorno vengano immesse nell'aria circa 10 milioni di tonnellate
di particolato; di queste il 94% è di origine naturale (nella foto a lato si
vedono gli effetti di un'enorme tempesta di sabbia nel deserto del Sahara). La
concentrazione nell'aria di queste particelle viene comunque limitata dalla
naturale tendenza alla deposizione per effetto della gravità e dall'azione
delle nubi o delle piogge (rimozione umida). Nell'aria pulita in genere la
concentrazione di questo inquinante è dell'ordine di 1-1,5 µg/mc.
Oltre che dalla natura dei venti e dalle precipitazioni la permanenza in
atmosfera è fortemente condizionata dalle dimensioni delle particelle. Quelle
che hanno un diametro superiore a 50 micrometri sono visibili nell'aria e
sedimentano piuttosto velocemente causando fenomeni di inquinamento su scala
molto ristretta.
Le
più piccole possono rimanere in sospensione per molto tempo; alla fine gli urti
casuali e la reciproca attrazione le fanno collidere e riunire assieme, in
questo modo raggiungono delle dimensioni tali da acquistare una velocità di
caduta sufficiente a farle depositare al suolo. Le polveri PM possono rimanere in sospensione per 12 ore circa, mentre
le particelle con un diametro inferiore ad 1 µm fluttuano nell'aria anche per 1
mese.
Il particolato emesso dai camini di altezza elevata può essere trasportato
dagli agenti atmosferici anche a grandi distanze. Per questo motivo parte
dell'inquinamento di fondo riscontrato in una determinata città può provenire
da un'industria situata a diversi Km dal centro urbano. Nei centri urbani
l'inquinamento da polveri fini (che sono le più pericolose per la salute) è
essenzialmente dovuto al traffico veicolare ed al riscaldamento domestico. Per
questo motivo, quando la concentrazione di particolato nell'aria diventa troppo
alta, vengono attuate delle limitazioni al traffico; in varie nazioni può anche
essere imposto un limite alla temperatura del riscaldamento negli ambienti
chiusi: 18°C in Germania o 20°C in Italia.
Effetti sull' uomo
A prescindere dalla tossicità, le particelle che possono produrre degli effetti indesiderati sull'uomo sono sostanzialmente quelle di dimensioni più ridotte, infatti nel processo della respirazione le particelle maggiori di 15 micron vengono generalmente rimosse dal naso. Il particolato che si deposita nel tratto superiore dell'apparato respiratorio (cavità nasali, faringe e laringe) può generare vari effetti irritativi come l'infiammazione e la secchezza del naso e della gola; tutti questi fenomeni sono molto più gravi se le particelle hanno assorbito sostanze acide (come il biossido di zolfo, gli ossidi di azoto, ecc.).
Per
la particolare struttura della superficie, le particelle possono anche
adsorbire dall'aria sostanze chimiche cancerogene; trascinandole nei tratti
respiratori e prolungandone i tempi di residenza, ne accentuano gli effetti. Le
particelle più piccole penetrano nel sistema respiratorio a varie profondità e
possono trascorrere lunghi periodi di tempo prima che vengano rimosse, per
questo sono le più pericolose. Queste polveri aggravano le malattie
respiratorie croniche come l'asma, la bronchite e l'enfisema.
Le persone più vulnerabili sono gli anziani, gli asmatici, i bambini e chi
svolge un'intensa attività fisica all'aperto, sia di tipo lavotrativo che
sportivo.
Nei luoghi di lavoro più soggetti all'inquinamento da particolato l'inalazione
prolungata di queste particelle può provocare reazioni fibrose croniche e
necrosi dei tessuti che comportano una broncopolmonite cronica accompagnata
spesso da enfisema polmonare.
effetti sull' ambiente
Gli
effetti del particolato sul clima e sui materiali sono piuttosto evidenti.
Il particolato dei fumi e delle esalazioni provoca una diminuzione della
visibilità atmosferica; allo stesso tempo diminuisce anche la luminosità
assorbendo o riflettendo la luce solare. Negli ultimi 50 anni si è notata una
diminuzione della visibilità del 50%, ed il fenomeno risulta tanto più grave
quanto più ci si avvicina alle grandi aree abitative ed industriali. Le polveri
sospese favoriscono la formazione di nebbie e nuvole, costituendo i nuclei di condensazione
attorno ai quali si condensano le gocce d'acqua. Di conseguenza favoriscono il
verificarsi dei fenomeni delle nebbie e delle piogge acide, che comportano
effetti di erosione e corrosione dei materiali e dei metalli.
Il
particolato inoltre danneggia i circuiti elettrici ed elettronici, insudicia
gli edifici e le opere d'arte e riduce la durata dei tessuti. Le polveri (ad
esempio quelle emesse dai cementifici), possono depositarsi sulle foglie delle
piante e formare così una patina opaca che, schermando la luce, ostacola il
processo della fotosintesi.
Gli effetti del particolato sul clima della terra sono invece piuttosto
discussi. Sicuramente un aumento del particolato in atmosfera comporta una
diminuzione della temperatura terrestre per un effetto di riflessione e
schermatura della luce solare, in ogni caso tale azione è comunque mitigata dal
fatto che le particelle riflettono anche le radiazioni infrarosse provenienti
dalla terra. E' stato comunque dimostrato che negli anni immediatamente successivi
alle più grandi eruzioni vulcaniche di tipo esplosivo (caratterizzate dalla
emissione in atmosfera di un'enorme quantità di particolato) sono seguiti degli
anni con inverni particolarmente rigidi. Alcune ricerche affermano che un
aumento di 4 volte della concentrazione del particolato in atmosfera
comporterebbe una diminuzione della temperatura globale della terra pari a
3,5°C.
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2025