|
|
| |
ESTRAZIONE E SEPARAZIONE MEDIANTE CROMATOGRAFIA
SU COLONNA DEI PIGMENTI DEGLI SPINACI
- Scopo dell'esperienza è estrarre e successivamente i pigmenti contenuti negli spinaci. La fase di estrazione verrà effettuata per semplice trituramento e aggiunta di una miscela di solventi, mentre la successiva separazione sarà imperniata sulla cromatografia su colonna e quindi su una ripartizione tra fasi. In più effettueremo un controllo della purezza di tali pigmenti rilevandone lo spettro e confrontandolo con quelli classici che vi sono associati. Le sostanze da estrarre e isolare presenti negli spinaci sono fondamentalmente di due tipi:
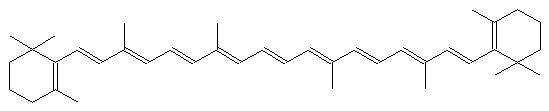
a) Il Beta-Carotene, colorato in giallo/arancio, è un carotenoide precursore della vitamina A; a livello strutturale è un polimero dell'isoprene.
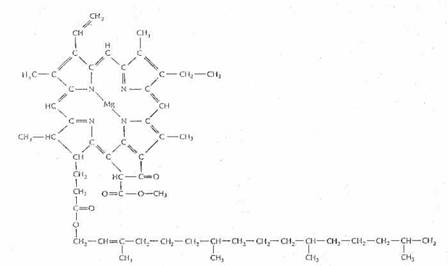
b) La Clorofilla, presente negli spina 919g61j ci nelle forme molecolari di clorofilla A e B, presenta un'intensa colorazione verde; E' una magnesio-porfirina, presentante cioè un centro metallico di magnesio all'interno di una struttura tetrapirrolica a sua volta caratterizzata da vari sostituenti.
- In più troviamo in modesta quantità delle Xantofille, cromaticamente affini al Beta-Carotene (e quindi tendenti al giallo) ma con peculiari differenze a livello chimico.
- Il sistema che utilizzeremo per separare le succitate sostanze, la cromatografia su colonna, è una procedura che permette di isolare le sostanze in base alla loro diversa affinità con sostanze più o meno polari; La colonna da cui prende il nome tale tecnica è un tubo di vetro nel quale sono poste sostanze chimiche in due fasi, una detta stazionaria (cioè solida) e una mobile (in stato di gas o come nel nostro caso di liquido). La fase stazionaria è completamente immersa in quella mobile e rappresenta la sostanza polare, solitamente carbonato di calcio o allumina, mentre la sostanza presente in stato liquido è molto meno polare e spesso volatile.
Se in un sistema di tale tipo viene posta una determinata sostanza, questa inizialmente si "depositerà" sulla fase stazionaria, determinando il fenomeno detto di adsorbimento dei soluti; successivamente, andando a eluire il tutto con la fase mobile che si sta utilizzando, si avrà l'attraversamento della fase stazionaria da parte della fase mobile.
 - Durante questo processo l'eluente, scarsamente polare, trascinerà con
sé eventuali sostanze che presentano una maggiore affinità per questa fase
mentre sostanze decisamente più polari preferiranno rimanere legate nella fase
polare stazionaria realizzando quindi una separazione fisica molto netta.
Macroscopicamente, se le sostanze da separare sono colorate, vedremo una
"striscia" scendere lungo la fase stazionaria man mano che questa viene
attraversata dall'eluente. Usando solventi a opportuna polarità è quindi
possibile far scendere preferenzialmente e con un certo scarto temporale le
sostanze che si preferisce, partendo da quella meno polare per poi strappare
alla fase anche quelle più polari usando eluenti sempre più "forti" in tal
senso.
- Durante questo processo l'eluente, scarsamente polare, trascinerà con
sé eventuali sostanze che presentano una maggiore affinità per questa fase
mentre sostanze decisamente più polari preferiranno rimanere legate nella fase
polare stazionaria realizzando quindi una separazione fisica molto netta.
Macroscopicamente, se le sostanze da separare sono colorate, vedremo una
"striscia" scendere lungo la fase stazionaria man mano che questa viene
attraversata dall'eluente. Usando solventi a opportuna polarità è quindi
possibile far scendere preferenzialmente e con un certo scarto temporale le
sostanze che si preferisce, partendo da quella meno polare per poi strappare
alla fase anche quelle più polari usando eluenti sempre più "forti" in tal
senso.
ESECUZIONE
- Poniamo circa 20g di spinaci in un mortaio dopo averli asciugati e parzialmente sminuzzati; aggiungiamo quindi con cautela (sotto cappa) circa 20ml di miscela di etere di petrolio 40-70° e acetone in rapporto di volume 4:1, un solvente quindi altamente infiammabile. Trituriamo finemente gli spinaci col pestello fino a produrre una colorazione intensamente verde e una fase organica ben distinta da quella sottostante acquosa, indice dell'avvenuta estrazione dei pigmenti degli spinaci; se necessario, vista l'elevata volatilità del solvente in uso, ne aggiungiamo ulteriore prima che gli spinaci rimangano a secco. Con una pipetta pasteur preleviamo quindi una piccola quantità di tale sospensione che sarà un mix di clorofilla, beta carotene e in minor parte di xantofilla.
- Prepariamo la colonna per la cromatografia, procedendo in quello che viene detto impiccamento della colonna. Al fondo, prima del rubinetto, poniamo un batuffolo di cotone idrofilo; quindi versiamo nella colonna quella che rappresenterà la nostra fase stazionaria, ovvero una sospensione di allumina neutra, ossido ceramico dell'alluminio (Al2O3), in etere di petrolio.
Effettuiamo tale operazione diverse volte, facendo depositare l'allumina sul fondo della colonna in numerosi strati e raccogliendo l'etere di petrolio percolante il solido; la sospensione di allumina si deposita nel modo più compatto possibile, evitando "buchi" che potrebbero compromettere la cromatografia offrendo vie di passaggio per le sostanze da adsorbire. A un'altezza di circa 8/9cm e con una buona stratificazione dell'allumina interrompiamo il processo, ponendo un secondo batuffolo di cotone idrofilo sulla sommità della fase stazionaria e avendo cura che il solvente sia a livello con tale barriera, garantendo quindi una copertura costante della fase stazionaria. Un corretto impiccamento è deducibile dalla velocità di fuoriuscita del solvente dal rubinetto sottostante la colonna, che se risulta molto più veloce di una goccia al secondo indica un insufficiente stratificazione dell'allumina.
- Aggiungiamo ora alla colonna la miscela di pigmenti prelevata dal mortaio, attendendo finchè la fase stazionaria non mostra un efficace adsorbimento dei soluti; a questo punto iniziamo la separazione vera e propria, aggiungendo in modo graduale alla colonna il nostro eluente cromatografico ovvero una miscela di etere di petrolio 40-70° e acetone stavolta in rapporto di volume 9:1. Tale fase mobile inizia a attraversare la colonna e, così facendo, trascina con sé le molecole di Beta Carotene; le clorofille, più polari, rimangono invece legate alla fase stazionaria in virtù della maggiore affinità. Macroscopicamente vediamo una linea gialla rappresentante il beta carotene che lentamente attraversa l'allumina, man mano che l'eluente percola la colonna. Giunta in prossimità del rubinetto poniamo un differente becher al di sotto della colonna, per raccogliere il pigmento e successivamente analizzarne la purezza.
- Una volta del tutto disceso il Beta Carotene andiamo a estrarre dalla colonna la clorofilla. Per far questo utilizziamo un solvente molto più polare che sia in grado di "strapparla" dalla fase stazionaria, ovvero una miscela di acetone e alcool metilico in rapporto di volume 30:1. Similmente a prima visualizziamo un'evidente banda verde in discesa, che raccogliamo in un altro becher una volta giunta al rubinetto; In più, notiamo una banda giallognola molto meno intensa del precedente Beta Carotene che rappresenta le tracce di Xantofilla in via di eliminazione anch'esse per trascinamento tramite la fase mobile.
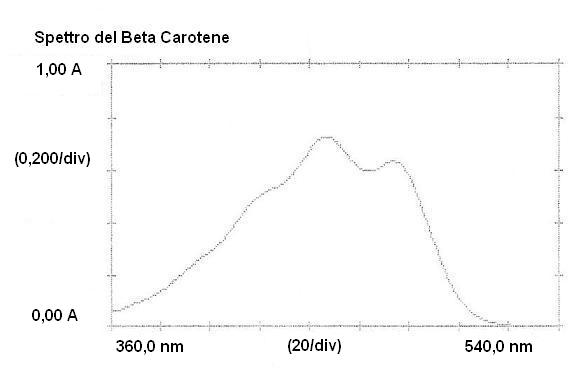
- Una volta ottenute in due becher le frazioni corrispondenti alle due bande e quindi ai due pigmenti, procediamo a effettuare un'analisi qualitativa della purezza; per far questo ci avvaliamo dello spettrofotometro. Per entrambe le sostanze prepariamo due cuvette con opportuni bianchi, essendo differenti i due eluenti utilizzati per sottrarre i pigmenti, e quindi andiamo a rilevare uno spettro di assorbimento impostando opportuni range di lunghezze d'onda nell'UV visibile: 360-540nm per il Beta Carotene e 400-700nm per la clorofilla.
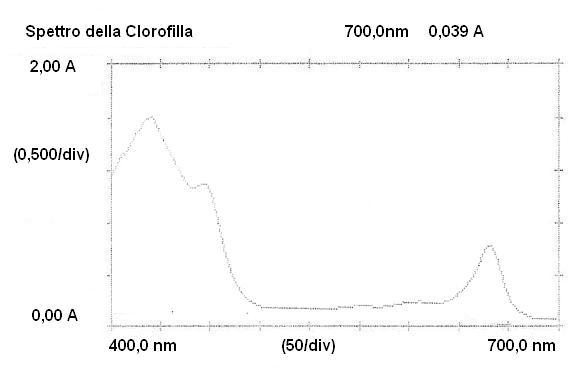
- I grafici ottenuti sono accettabilmente coerenti con gli spettri classici di tali sostanze riportati in letteratura e con discreti picchi per quanto riguarda la concentrazione; nello spettro registrato della clorofilla si evidenzia un picco "anomalo" tra i 400/450nm dovuto a impurezze causate da tracce di Beta Carotene e Xantofille frammiste alla sostanza in esame.
PICCHI DI ASSORBIMENTO
Beta Carotene Clorofilla
474.0 nm ABS 0.630 662.5 nm ABS 0.587
447.0 nm ABS 0.724 470.0 nm ABS 1.022
433.0 nm ABS 1.516
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2026