|
|
| |
METODOLOGIA
Frazionamento cellulare
Si tratterà della metodologia attraverso la quale sia possibile studiare il materiale contenuto all'interno della cellula. Prevede un tessuto sul quale si opera un frazionamento allo scopo di recuperare le singole parti:
Si rompono le singole cellule che si trovano nel tessuto: si ricorre ad oggetti che permettano l'omogeneizzazione. Per far esplodere il tessuto si una un contenitore ed un pestello: lucido. Nel contenitore si mette un liquido (acqua o soluzione tampone ipertonica) poi si introduce il campione di tessuto che viene pestato con un motorino collegato al pestello (il contenitore viene messo nel ghiaccio tritato per compensare il calore che altrimenti rovinerebbe il campione). Tutto ciò porta ad ottenere una "pappetta" simile ad un omogeneizzato.
Si lascia riposare per 20 minuti affinché l'omogeneizzato abbia il tempo di dividersi in due parti di differente consistenza: pellet che è il sedimento costituito dalle componenti cellulari più pesanti e supernatante.
Viene recuperato il supernatante per essere centrifugato attraverso una centrifuga che crea un campo gravitazionale (g) tot volte più alto del normale. Si ottengono così:
nuclei a 1000 g per 20 minuti
mitocondri, lisosomi, perossisomi a 10.000 g per 20 minuti
microsomi a 105.000 g per 120 minuti
reticolo endoplasmatico occorre una ultracentrifuga.
ribosomi occorre disgregare il "piedistallo" dei ribosomi cioè una
struttura membranosa composta da lipidi e proteine, aggiungendo
un detergente: sodio desossicolato al 0,26% a 105.000 g per 20
minuti.
Uso degli isotopi in biologia e medicina
Gli isotopi sono variazioni di elementi chimici: pur occupando lo stesso posto nella tavola periodica hanno un diverso numero di neutroni che li rende riconoscibili e traccianti, caratteristica che viene sfruttata per conoscere il destino di composti introdotti nella cellula: per esempio N è l'atomo normale, il suo isotopo è N.
Gli isotopi vengono riconosciuti ed accettati dall'organismo per il loro assetto elettronico che è il responsabile della reazione chimica. Però l'isotopo, una volta introdotto nell'organismo, può essere seguito, in quanto è tracciante o marcatore: per esempio un glucosio con atomi di carbonio C una volta trovatosi nell'organismo conduce l'osservatore attraverso le varie fasi metaboliche a cui va incontro.
Gli isotopi usati in biologia e medicina sono:
stabili: non emettono radiazioni
radioattivi: emettono radiazioni che impressionano una lastra fotografica.
Gli isotopi radioattivi sono quelli più usati perché anche se presenti in piccolissime quantità permettono di essere identificati. Il composto chimico al quale si è aggiunto un isotopo prende il nome di composto marcato. Tutte le conoscenze sulle vie metaboliche si devono agli isotopi.
Esempio di esperimento attuato con l'uso degli isotopi:
Lo scopo dell'esperimento è verificare che le proteine vengano sintetizzate a livello del reticolo endoplasmatico rugoso.
Ad un animale si iniettano i 20 aminoacidi di cui alcuni sono marcati con C. Si lascia passare il tempo che occorre per la sintesi proteica e si trovano alcune proteine radioattive.
Si prendono le proteine e si sottopongono a elettroforesi e a radiografia. Dopo un po' la lastra fotografica rimane impressionata dalle radiazioni delle proteine così marcate.
Oltre a questo si fa un'ulteriore verifica del tessuto con una preparazione istologica spennellata con emulsione fotografica: il preparato verrà poi avvolto e riposto per essere recuperato dopo qualche tempo durante il quale si formeranno macchie scure. Questa tecnica è l'autoistoradiografia.
Medicina diagnostica: gli isotopi sono usati per esempio per verificare la funzionalità della tiroide (ghiandola che cattura lo iodio). Viene iniettato al paziente una soluzione contenete iodio radioattivo e dopo un po' di tempo viene fatta appoggiare una lastra fotografica sulla zona tiroidea. La lastra sarà impressionata con la forma della tiroide intera se il paziente non ha disfunzioni in questo senso. Se invece la tiroide funziona solo in parte, solo la zona sana impressionerà la lastra.
Recentemente è stato messo a punto un metodo per individuare le cellule tumorali del cervello attraverso tecnezio radioattivo, isotopo capace di legarsi alle cellule tumorali tipiche di quella zona.
Alcuni tipi di isotopi comunemente usati come traccianti
|
Elemento normale |
Peso atomico relativo |
Isotopo |
Attività |
Vita media |
Radiazione connessa |
|
H |
|
H |
stabile |
|
|
|
|
|
H |
radioattivo |
12,1 anni |
beta |
|
C |
|
C |
radioattivo |
5700 anni |
beta |
|
N |
|
N |
stabile |
|
|
|
O |
|
O |
stabile |
|
|
|
P |
|
P |
radioattivo |
14,3 gg |
beta |
|
S |
|
S |
radioattivo |
87,1 gg |
beta |
|
I |
|
I |
radioattivo |
8 gg |
beta, gamma |
|
|
|
I |
radioattivo |
60 gg |
daniele |
Riepilogo delle fasi di autoistoradiografia:
Cellule vive vengono esposte al tracciante radioattivo;
Le suddette cellule vengono lavate per togliere l'eccesso di radiazioni;
Le sezioni vengono deposte su un vetrino portaoggetti;
I vetrini vengono asciugati e tenuti al buio. Durante questo periodo si verifica l'esposizione dei cristalli dell'emulsione fotografica che si trovano in corrispondenza dei punti della sezione che emette radioattività. Questo avviene perché la biomolecola incorpora il procursore radioattivo o caldo.
Proprietà fisico chimiche degli acidi nucleici
Gli acidi nucleici esibiscono una particolare caratteristica fisico chimica che è quella di assorbire le radiazioni ultraviolette. Questo particolarità consente di valutare la presenza di questi composti chimici che altrimenti risulterebbero del tutto invisibili.
260 millimicron risulta essere il picco massimo d'assorbimento
degli acidi nucleici, e cioè in corrispondenza delle radiazioni
ultraviolette.![]()
![]()
![]()
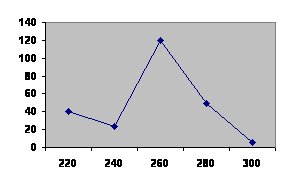
Le normali pratiche istologiche permetto di legare coloranti specifici agli acidi nucleici, ma in tal caso la molecola andrebbe incontro a modificazioni o alla rottura, il che non ne permetterebbe un uso successivo.
L'assorbimento delle radiazioni ultraviolette avviene in quanto gli acidi nucleici hanno una struttura aromatica che quindi presenta 3 doppi legami delocalizzati che hanno questa speciale qualità.
Individuazione dell'autoreplicazione del DNA
Nella autoreplicazione del DNA popolazioni macromolecolari possono essere individuate tramite ultracentrifugazione in un mezzo nel quale si sono creati gradienti di concentrazione.
Procedura:
solitamente viene utilizzata una provetta morbida di acetato di cellulosa. Per esempio utilizzando un comune bicchiere per costituire un gradiente di solubilità, possiamo versare sul fondo del bicchiere una soluzione formata da acqua e zucchero in grandissime quantità, successivamente nello stesso bicchiere viene aggiunta una nuova soluzione contenente una percentuale di zucchero inferiore alla precedente, questo viene fatto più di una volta; adesso notiamo, guardando il bicchiere, uno stratificarsi delle diverse soluzioni, abbiamo creato un gradiente di densità discontinuo. In biologia si utilizzano gradienti continui, cioè senza linee di separazione, formati o da saccarosio molto concentrato, oppure da una soluzione salina formata con del cloruro di cesio (CsCl). Vengono utilizzate soluzioni molto concentrate, immesse nella provetta di acetato di cellulosa che successivamente viene sottoposta ad ultracentrifugazione. Dopo molte ore di rotazione le forze centrifughe riescono a separare le particelle di CsCl, dopo 48 ore si formerà un gradiente continuo salendo verso il culmine della provetta le particelle di cesio diminuiranno. Con il procedimento sopra descritto è possibile separare i singoli componenti di una miscela di macromolecole in base alla loro densità.
Separazione degli acidi nucleici in base alla loro densità
Il procedimento prevede il mescolamento di campioni di acidi nucleici nel CsCl, la sua ultracentrifugazione, e la sua successiva divisione in base alle taglie macromolecolari degli acidi nucleici in esso disciolti. Questo metodo permette di individuare tre tipi diversi di acidi nucleici, che osservati sotto luce ultravioletta appaiono come tre strisce orizzontali nella provetta.

![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Densità di flottazione
Il grafico è dato da un sistema di registrazione automatico, e dal numero dei "picchi" siamo in grado di notare che ci sono tre tipi di acidi nucleici diversi, questo procedimento è in grado di scegliere un particolare tipo di acido nucleico, recuperarlo e successivamente poterlo manipolare; difatti in prossimità della striscia di acido nucleico interessata, viene forata la provetta con una siringa ed aspirato l'acido nucleico interessato.
Ci possono essere altri sistemi molto più automatizzati per recuperare le singole zone, il foro viene effettuato sul fondo della provetta con un ago che farà sgocciolare partendo dal fondo il contenuto della stessa, la sospensione verrà recuperata da piccoli contenitori adagiati su un carrellino, che scorrerà ad una velocità precisamente calcolata. Poi viene effettuata sui campioni raccolti dai piccoli contenitori interessati una ultracentrifugazione in gradiente di densità (come quella sopra descritta).
Sistema per dimostrare la doppia elica del DNA
Consente di provare in modo inequivocabile la struttura bicatenaria del DNA. Watson e Crick usufruendo dei cristallogrammi, testando la composizione chimica, fisica e la vischiosità del materiale, riuscirono proprio con la tecnica sopra utilizzata a dimostrare che la vischiosità varia e di conseguenza, gli acidi nucleici modificando le radiazioni ultraviolette assorbite, sono strutture bicatenarie
Proprietà del DNA: la denaturazione
![]()
![]()
![]()
![]()
![]()
![]()
![]() Come per le proteine
la struttura terziaria degli acidi nucleici può essere modifica, e di
conseguenza possono essere rotte le interazioni deboli e forti che faranno
svolgere il filamento poliptidico con il procedimento del
"random-coil". Normalmente la stabilità del DNA è assicurata da
legami deboli che tengono unite le singole parti dell'acido
desossiribonucleico, reazioni chimiche e fisiche possono separare e far
distendere i filamenti. W. e C. usarono il calore per denaturare il DNA (agente
fisico)
Come per le proteine
la struttura terziaria degli acidi nucleici può essere modifica, e di
conseguenza possono essere rotte le interazioni deboli e forti che faranno
svolgere il filamento poliptidico con il procedimento del
"random-coil". Normalmente la stabilità del DNA è assicurata da
legami deboli che tengono unite le singole parti dell'acido
desossiribonucleico, reazioni chimiche e fisiche possono separare e far
distendere i filamenti. W. e C. usarono il calore per denaturare il DNA (agente
fisico)

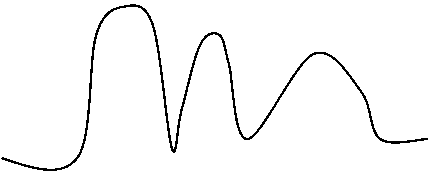
1,4
![]()

1,0
40 50 60 70 80 90 C°
A 40 °C si registra un valore d'assorbimento uguale a 1
A 50 °C si registra un valore di assorbimento uguale a 1
a 70 °C c'è una forte "impennata" della curva e notiamo che l'assorbimento è aumentato tantissimo, difatti rasenta 1,5 (40 -50 % in più rispetto a temperature normali). A 80 -90 °C l'assorbimento cessa d'aumentare, il DNA è ora denaturato e i due filamenti si sono separati.
La spiegazione per la quale aumenta l'assorbimento dei raggi ultravioletti, è quella perchè le basi azotate quando sono fra loro accoppiate si trovano "sequestrate" all'interno dell'elica, di conseguenza quando l'elica si separa le basi azotate (anelli aromatici) sono più esposte ed è per questo motivo che aumenta l'assorbimento.
Il percorso di denaturazione è reversibile, cioè può essere svolto a ritroso, ricomporre nuovamente il DNA nella forma nativa (rinaturazione) è un'operazione molto delicata e difficile, occorre ritornare alla temperatura iniziale molto graduatamente, cioè effettuare un raffreddamento molto lento. I due filamenti complementari, disciolti in una soluzione acquosa (il DNA è una molecola sempre idratata), ricombaciano in maniera perfetta (tipo una cerniera lampo).
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2025