|
|
| |
|
SINTESI ACIDO para-NITROBENZOICO |
Scopo: sintetizzare l'acido para-nitrobenzoico partendo dal para-nitrotoluene e determinarne il punto di fusione.
Cenni teorici: per sintetizzare l'acido paranitrobenzoico partendo dal paranitrotoluene occorre effettuare una reazione di ossidazione ovvero fare in modo che il carbonio del gruppo CH3 cambi numero di ossidazione ad uno più elevato. In questo caso specifico la ossidazione viene effettuata con permanganato di potassio (KMnO4), specie molto ossidante in grado di portare il carbonio da -3 a +3 e di ridursi a biossido di manganese MnO2.
La reazione che avviene, stechi 919j99j ometricamente bilanciata, è la seguente:
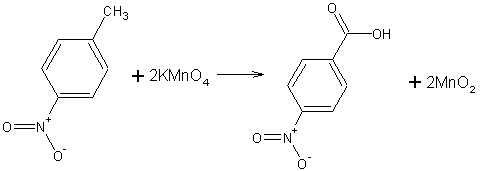
La reazione va fatta a caldo (circa 200°C) e sotto continua agitazione, con un difetto di permanganato affinché reagisca completamente per poi aggiungerlo goccia a goccia tramite la buretta posta sull'apparecchiatura. Il tubo a ricadere serve per condensare il vapore acqueo e fare in modo che la soluzione non si concentri troppo.
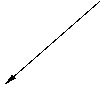
L'apparecchiatura per l'ossidazione dell'para-nitrotoluenene ad acido para-nitrobenzoico è composta secondo questo schema:
Tubo refrigerante ad acqua Pallone
contenente para-nitrotoluene Buretta contenente KMnO4 Raccordo di Claisen


 L'acido
paranitrobenzoico di formula C7H5NO4 ha un
peso molecolare di 167 g/mol ed un punto di fusione di 239 °C.
L'acido
paranitrobenzoico di formula C7H5NO4 ha un
peso molecolare di 167 g/mol ed un punto di fusione di 239 °C.
E' un acido carbossilico debole monoprotico insolubile in acqua a freddo, più solubile a caldo.
Si presenta come un solido di colore bianco sottoforma di cristalli aghiformi.
Materiale usato:
Pallone in vetro da 250 ml
Raccordo di Claisen
Tubo refrigerante ad acqua
Tubi in plastica
Ancoretta magnetica
Buretta con raccordo normalizzato
Imbuto di Buchner
Carta da filtro
Capillare in vetro
Apparecchiatura per calcolo punto fusione
Agitatore a piatto riscaldante
Acido cloridrico 37%
Paranitrotoluene
Permanganato di potassio KMnO4 solido
Acqua distillata
Spruzzetta per acqua
Ghiaccio
Termometro
Bilancia tecnica ( 0.01g)
Bacchetta in vetro
Cloruro di sodio
Vetrino d'orologio
Cristallizzatore
Imbuto a doppia intercapedine
Procedimento: si pongono a reagire 3g di para-nitrotoluene nel pallone di vetro con 3,5g circa di permanganato di potassio e 35ml di acqua distillata assieme all'ancoretta per mantenere agitata la soluzione durante la reazione.
Si riscalda cautamente su piastra riscaldante e si pone nella buretta di carica la soluzione restante di permanganato e si fa scendere lentamente in un tempo di 30 minuti.
Una volta che tutto il permanganato di potassio, necessario per ossidare tutto il para-nitrotoluene, è stato aggiunto si riscalda ancora per 60 minuti e negli ultimi minuti si alza bruscamente la temperatura per spingere la reazione.
Si filtra a caldo su imbuto a doppia intercapedine e si lava il filtro, contenente il biossido di manganese, con piccole quantità d'acqua calda.
Si riscalda la soluzione, che dopo la filtrazione dovrebbe aver assunto un colore giallino, e si aggiungono 2ml di HCl concentrato per desalificare l'acido para-nitrobenzoico e quindi farlo precipitare (siccome nella forma acida è poco solubile).
Se la soluzione appena filtrata presentasse una colorazione violetta (presenza di permanganato non reagito) con l'aggiunta di acido cloridrico scompare.
Si lascia raffreddare naturalmente e si filtra la soluzione su imbuto di Buchner lavando il precipitato con acqua precedentemente raffreddata in un bagno di ghiaccio e sale.
Si pone per qualche minuto il filtro con il precipitato in stufa e si determina la resa percentuale ed il punto di fusione.
Elaborazione dati:
Calcolo grammi permanganato di potassio necessari per fare reagire 3g di para-nitrotoluene:
PM para-nitrotoluene = 137,15g/mol
Moli para-nitrotoluene = 3g / 137,15g/mol =0,0219 mol
Moli KMnO4 = 2 * 0,0219 mol = 0,0438 mol
Grammi KMnO4 = 0,0438 mol * 158,04 g/mol = 6,92 g
Si prende un leggero eccesso di KMnO4 (+2-3%) quindi si dovranno pesare:
7,1g
Calcolo resa di reazione:
PM acido para-nitrobenzoico = 167g/mol
Grammi teorici di acido para-nitrobenzoico = 0,0219 mol * 167g/mol = 3,66g
Grammi filtro di carta = 0,52g
Grammi filtro + ppt = 2,31g
Grammi ppt = 1,79g
Resa % = 1,79g / 3,66g * 100 = 49 %
Calcolo intervallo di fusione (punto di fusione):
PF teorico = 239°C
PF pratico = 240° C
Conclusioni: lo scopo dell'esperienza, sintetizzare l'acido para-nitrobenzoico partendo dal para-nitrotoluene e determinarne il punto di fusione, è stato raggiunto seppure con una resa di reazione molto bassa 49%.
Una resa cosi bassa è probabilmente dovuta al fatto che, durante la filtrazione, la soluzione e l'imbuto a mantello riscaldante non erano sufficientemente caldi e quindi è probabile che una parte di acido para-nitrobenzoico abbia cristallizzato nel filtro contenente il biossido di manganese.
La soluzione filtrata, presentava una colorazione violetta perché vi era del permanganato di potassio in eccesso ma, con l'aggiunta di acido cloridrico 37%, questa è sparita senza lasciare tracce di MnO2 perché il permanganato è stato ridotto, dallo ione Cl-, nella forma ionica Mn2+ perfettamente solubile in acqua.
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2024