|
|
| |
FINALITA':
III. Determinare la solubilità in H2O e in CH3CH2OH di sostanze organiche contenenti proteine
MATERIALI e STRUMENTI:
Fornello elettrico
Becher
Frullatore
Mortaio
Provette
Portaprovette
Portaprovette da bagnomaria
Latte
Albume d'uovo
Carne
Pane
Acqua
Saggio al biureto (Soluzione A + Soluzione B)
Soluzione A (Cu2SO4)
Soluzione B (NaOH)
Etanolo (CH3CH2OH)
Acido nitrico (HNO3)
Le proteine sono molecole organiche che costituiscono gran parte di un organismo vivente e sono costituite da lunghe sequenze di amminoacidi. Gli amminoacidi sono caratterizzati dalla presenza di un gruppo amminico (NH2) e di un gruppo carbossilico (COOH). Venti di questi composti (alanina, arginina, asparagina, acido aspartico, cisteina, acido glutammico, glutammina, glicina, istidina, isoleucina, leucina, lisina, metionina, fenilalanina, prolina, serina, treonina, triptofano, tirosina e valina) sono chiamati alfa-amminoacidi e costituiscono tutte le proteine. La loro formula generale è:
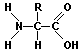
Il gruppo amminico e quello carbossilico sono entrambi legati allo stesso atomo di carbonio, detto carbonio alfa, che porta un gruppo (R) variabile. Nel più semplice degli amminoacidi, la glicina, il gruppo R è costituito da un solo atomo di idrogeno, mentre tutti gli altri amminoacidi presentano gruppi R più complessi, che possono contenere atomi di carbonio, idrogeno, ossigeno, azoto e zolfo.
Durante la sintesi delle proteine, che avviene all'interno delle cellule, il gruppo carbossilico (COOH) di un amminoacido reagisce con il gruppo amminico(NH2) di un altro, formando un legame peptidico (CO-NH).Questa reazione avviene per un gran numero di amminoacidi, che formano così una lunga catena, detta polipeptide. Un polipeptide può contenere un numero di amminoacidi variabile fra 50 e varie centinaia. Le proteine sono in genere costituite da una singola catena polipeptidica o da più catene, unite fra loro da deboli legami molecolari; la sequenza degli amminoacidi di ciascuna catena viene specificata da precise istruzioni localizzate nel materiale genetico delle cellule. Le combinazioni pressoché infinite in cui si possono allineare gli amminoacidi e la forma tridimensionale che può assumere il filamento proteico contribuiscono a spiegare la grande diversità di compiti svolti dalle proteine negli organismi viventi. La sequenza lineare degli amminoacidi determina la cosiddetta struttura primaria delle proteine e contribuisce alla loro forma tridimensionale. Tra i diversi amminoacidi presenti in vari punti della catena si possono, infatti, instaurare diversi tipi di legami chimici, i quali determinano l'avvolgimento o il ripiegamento della struttura della proteina nelle due possibili varianti della struttura secondaria: a elica o a foglietto. Quando queste strutture di tipo secondario si ripiegano ulteriormente, si forma una proteina a struttura terziaria. Le proteine formate da più catene polipeptidiche, tenute insieme da legami chimici di diversa natura, presentano struttura quaternaria; esempi sono l'emoglobina e numerosi enzimi.Le proteine si possono classificare in due categorie: proteine fibrose e proteine globulari. Tra le più importanti proteine fibrose vi sono il collagene, la cheratina, il fibrinogeno e le proteine muscolari. A differenza dalle proteine fibrose, le proteine globulari sono sferiche e molto solubili. Esempi di queste proteine sono l'albumina, le globuline, la caseina, l'emoglobina, tutti gli enzimi e gli ormoni proteici.
PROCEDIMENTO
Portare in soluzione liquida carne e pane
Versare 5 ml di ogni sostanza in quattro provette
Aggiungere venti gocce di soluzione A e venti di soluzione B
Verificare il colore di ogni provetta
Scaldare a bagnomaria le provette per alcuni minuti
Ricontrollare il colore e registrare i risultati
Sostanza |
Colore a temperatura ambiente |
Colore finale |
|
LATTE |
viola |
arancio-marrone |
|
PANE |
blu |
arancio-marrone |
|
ALBUME |
blu |
viola |
|
CARNE |
viola |
viola |
In questa esperienza abbiamo utilizzato due sostanze per verificare la presenza di proteine: ci siamo avvalsi del fatto che l'idrossido di sodio riesca a spezzare i legami peptidici, e il solfato di rame viri verso un colore viola se questa reazione è avvenuta. Nel nostro caso l'esito della prova è positivo in tutti i casi, infatti il colore finale delle soluzioni è viola per l'uovo e per la carne, mentre il colore arancio-marrone del latte e del pane evidenzia, oltre a quella delle proteine, anche la presenza di zuccheri. Nell'esperienza con il saggio di Benedict abbiamo infatti avuto una reazione molto simile con il latte che alla fine dell'esperimento risultava di un colore arancio-marrone.
Versare in quattro provette 2ml delle stesse sostanze della prova I
Aggiungere in ognuna dieci gocce di acido nitrico
Scaldare le provette a bagnomaria per venti minuti circa
Controllare il colore assunto da ogni soluzione
Sostanza |
Colore |
|
LATTE |
giallo paglierino |
|
PANE |
bianco |
|
ALBUME |
giallo |
|
CARNE |
rosa tendente al giallo |
Il colore assunto da carne e latte era tendente al giallo, e ciò ci può far pensare che contengano proteine aromatiche, ma non ne siamo completamente sicuri. Il pane non contiene sicuramente proteine di questo tipo, mentre per l'uovo non siamo stati in grado di decidere, in quanto in condizioni normali l'albume d'uovo è giallo. Le proteine aromatiche sono proteine costituite da amminoacidi come fenilalanina e il triptofano che hanno nel loro gruppo R anelli di carbonio (in questo caso, detti appunto anelli aromatici).
Prendere 2 ml di ogni sostanza e versarla nelle provette
Aggiungere 5 ml di acqua
Verificare se le sostanze sono o no solubili
Prendere 2 ml di ogni sostanza e versarla nelle provette
Aggiungere 5 ml di etanolo
Verificare se le sostanze sono o no solubili
|
Sostanza |
Solubilità in acqua |
Solubilità in alcool etilico |
LATTE |
Molto solubile |
Non solubile |
|
PANE |
Solubile |
Non solubile |
|
ALBUME |
Poco solubile |
Non solubile |
|
CARNE |
Solubile |
Non solubile |
La non solubilità delle sostanze in alcool etilico era abbastanza scontata, in quanto è una sostanza poco polare, mentre l'acqua è polare. Una legge riguardante la solubilità, dice che due soluzioni simili (polare-polare e apolare-apolare) sono solubili tra di loro, mentre due soluzioni eterogenee non sono solubili.
|
Privacy |
Articolo informazione
Commentare questo articolo:Non sei registratoDevi essere registrato per commentare ISCRIVITI |
Copiare il codice nella pagina web del tuo sito. |
Copyright InfTub.com 2024